厦门大学“电化学研究范式”线上暑期学校

主讲人 · 孙世刚院士

中国科学院院士,国家级教学名师。
获中国电化学会首届“中国电化学贡献奖”、国际车用锂电池协会“终身成就奖”、国际电化学会 “Brian Conway”奖章、国家自然科学奖二等奖等奖项。担任Electrochimica Acta、《化学学报》等学术期刊副主编、《电化学》主编。


一、引论
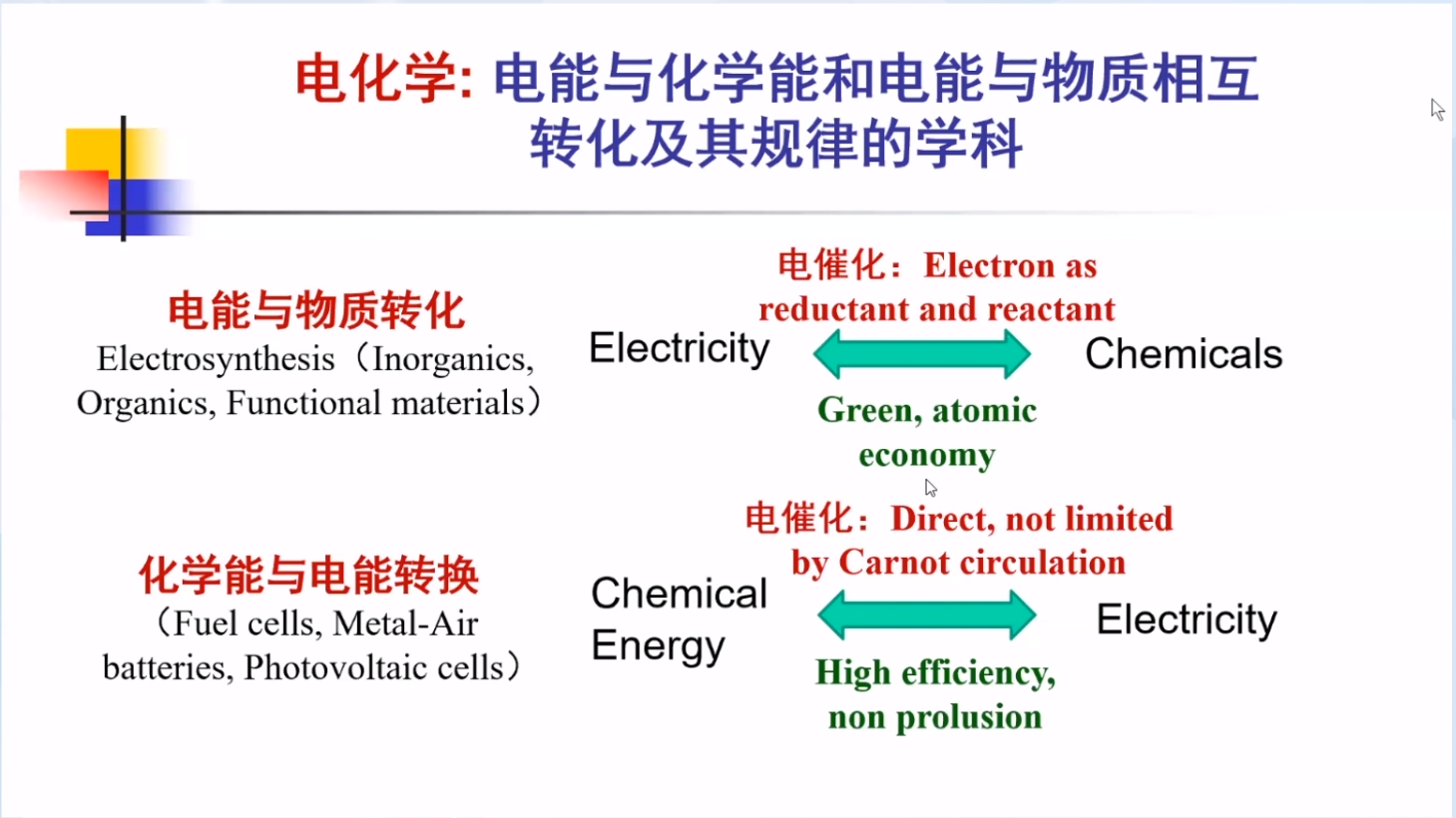
电化学方法的特点:电子作为氧化剂/还原剂促使物质、能量的转化。
电化学能源的优势:绿色、原子经济;直接转化电能和化学能,不受热力学卡诺循环限制,高转化效率;零排放、无污染;可靠、灵活、安全、少维护、长寿命、应用广泛。
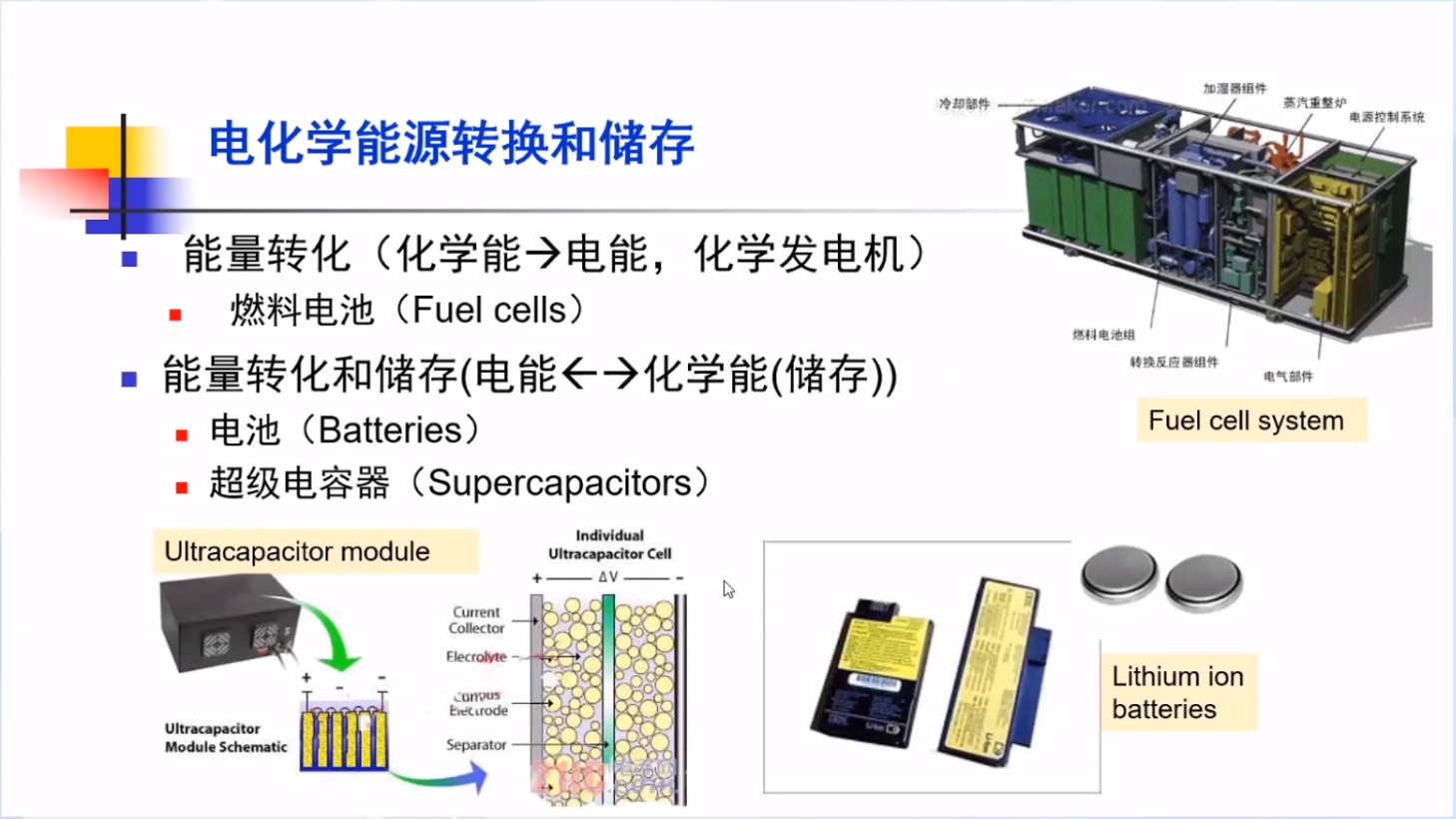
电化学能源促进可再生能源开发利用→间歇式能源储存
电化学能源推动新能源汽车发展和CO2减排→锂离子电池系统更适合替代汽油机,氢燃料电池系统更适合替代柴油机。
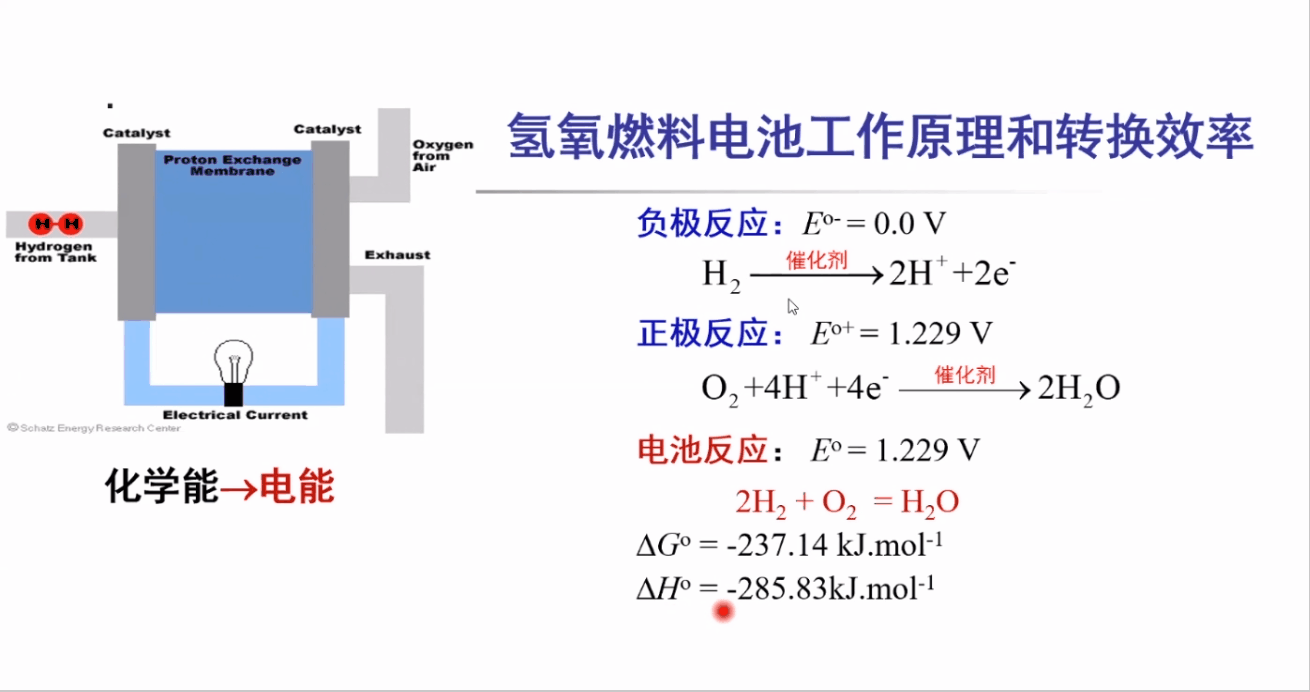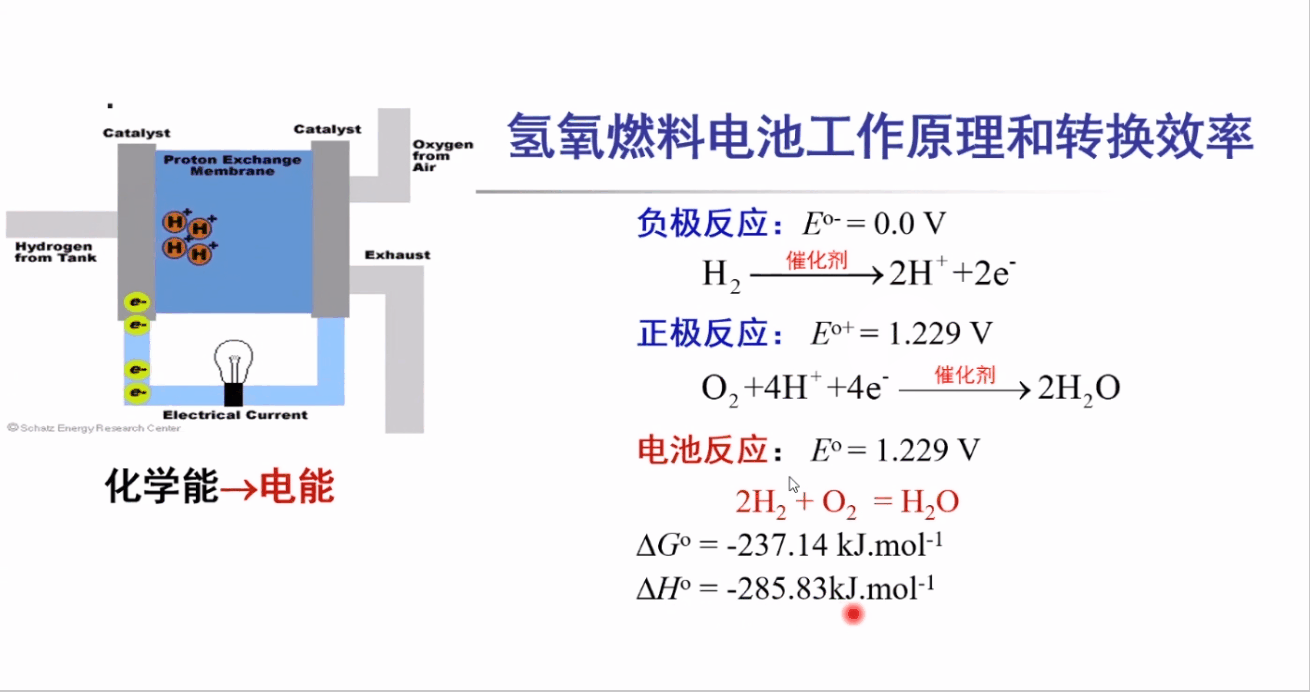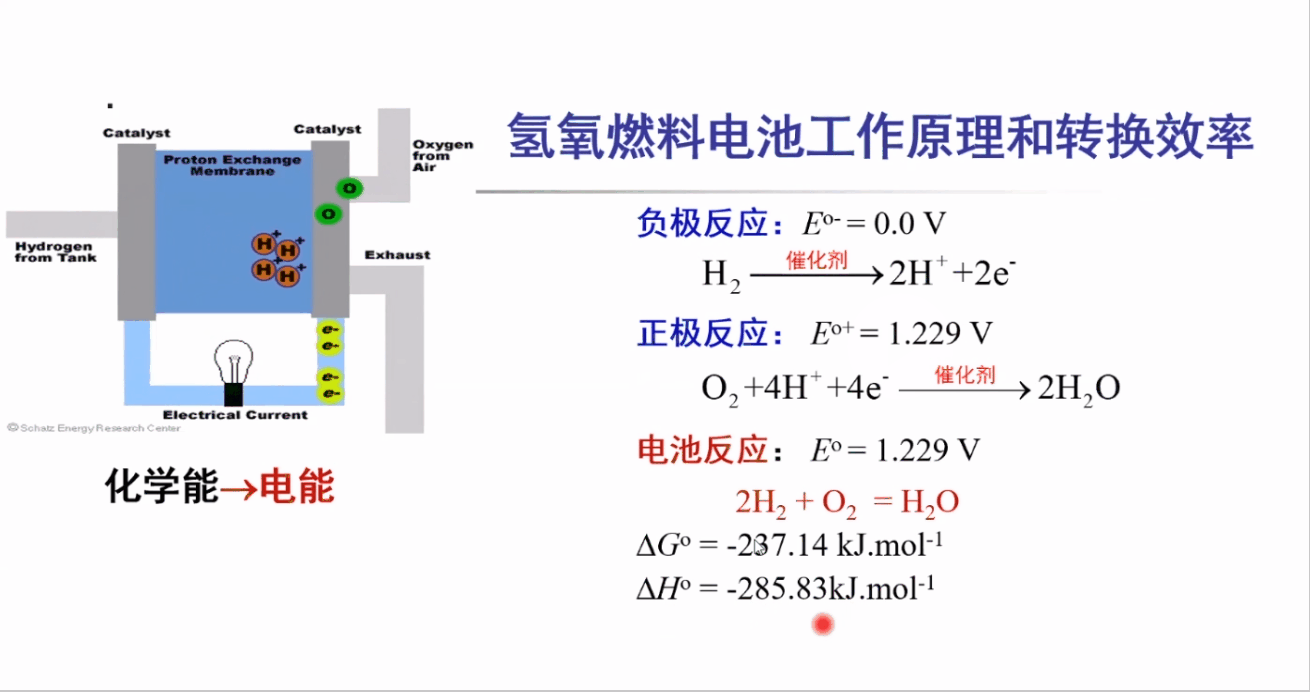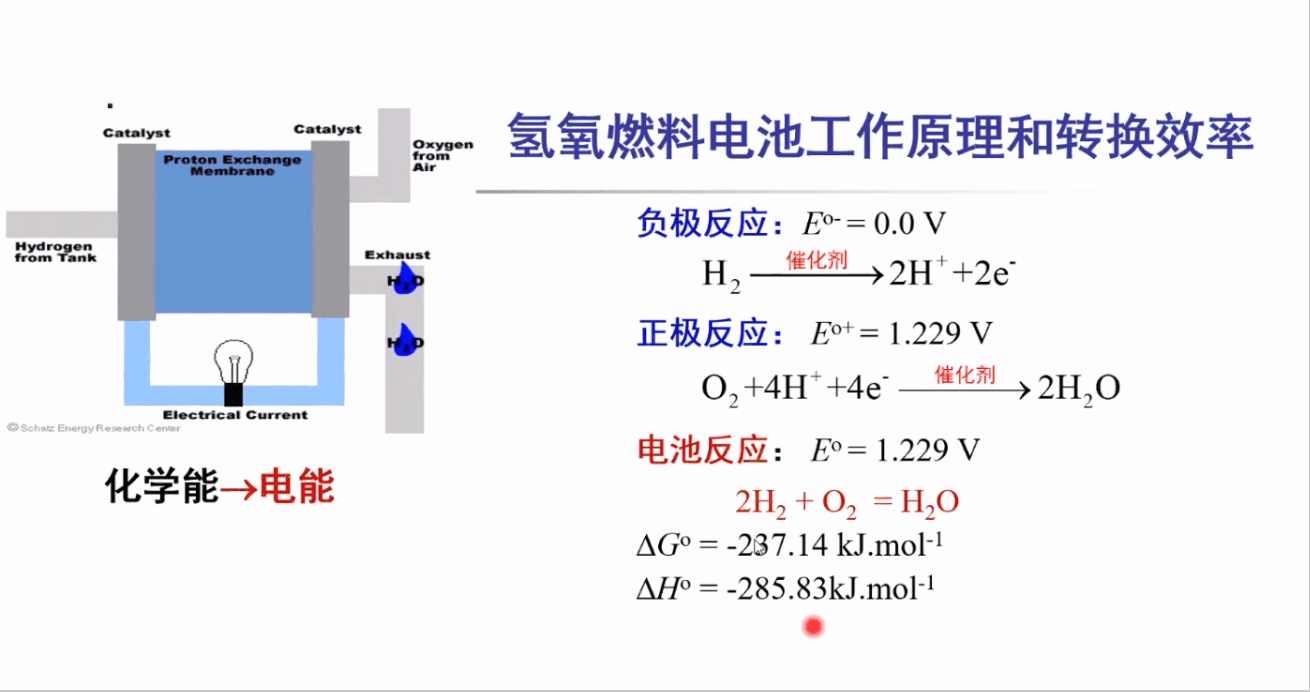
氢氧燃料电池的工作原理:
阳极反应(负极反应):HOR(氢的氧化)
阴极反应(正极反应):ORR(氧的还原)
通常条件下,此反应可自发进行,但速度极慢。
在燃料电池中可通过使用催化剂促进反应快速进行。

电催化和催化的区别:
电催化:电催化剂+电子传递;固液界面、固固界面、液液界面;通过改变界面电场来调控体系能量(大部分常温常压即可实现)。
催化:催化剂+化学反应;固气界面,均相反应(溶液);通过改变温度、改变压力来调控体系能量。
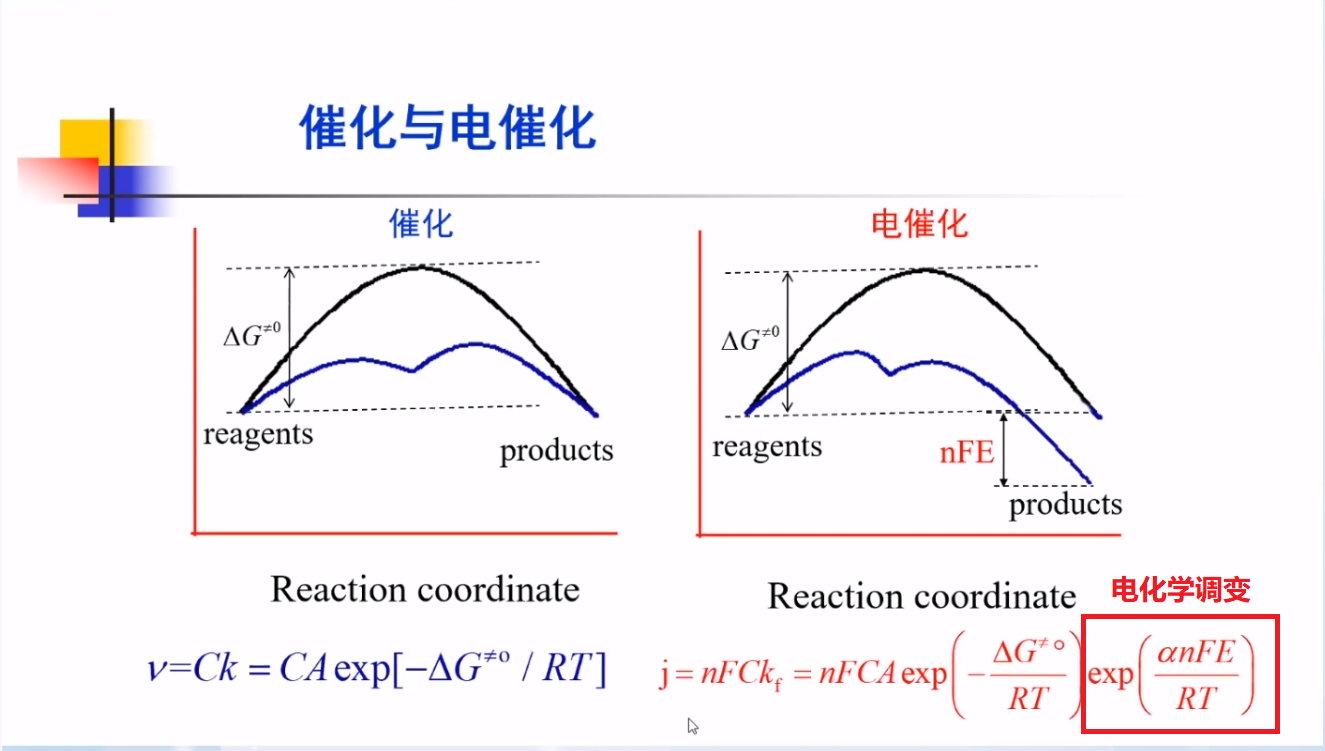
从能量角度分析催化和电催化的特点:
催化:通过改变反应途径降低本征能垒;
电催化:通过改变反应途径降低本征能垒;通过控制界面电场、控制电极电位进一步降低能垒。
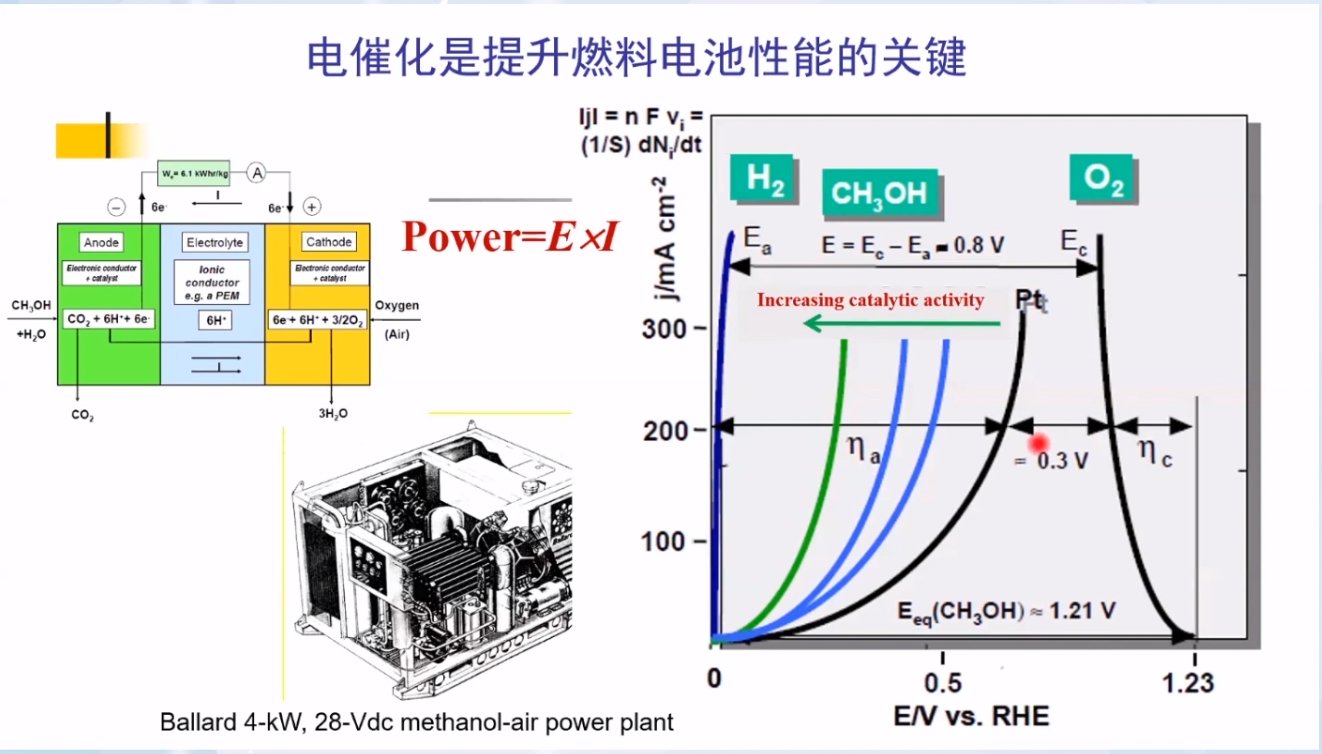
电催化是提升燃料电池性能的关键。催化剂的加入可以使阳极的极化曲线发生移动,从而对外输出更高的功率。
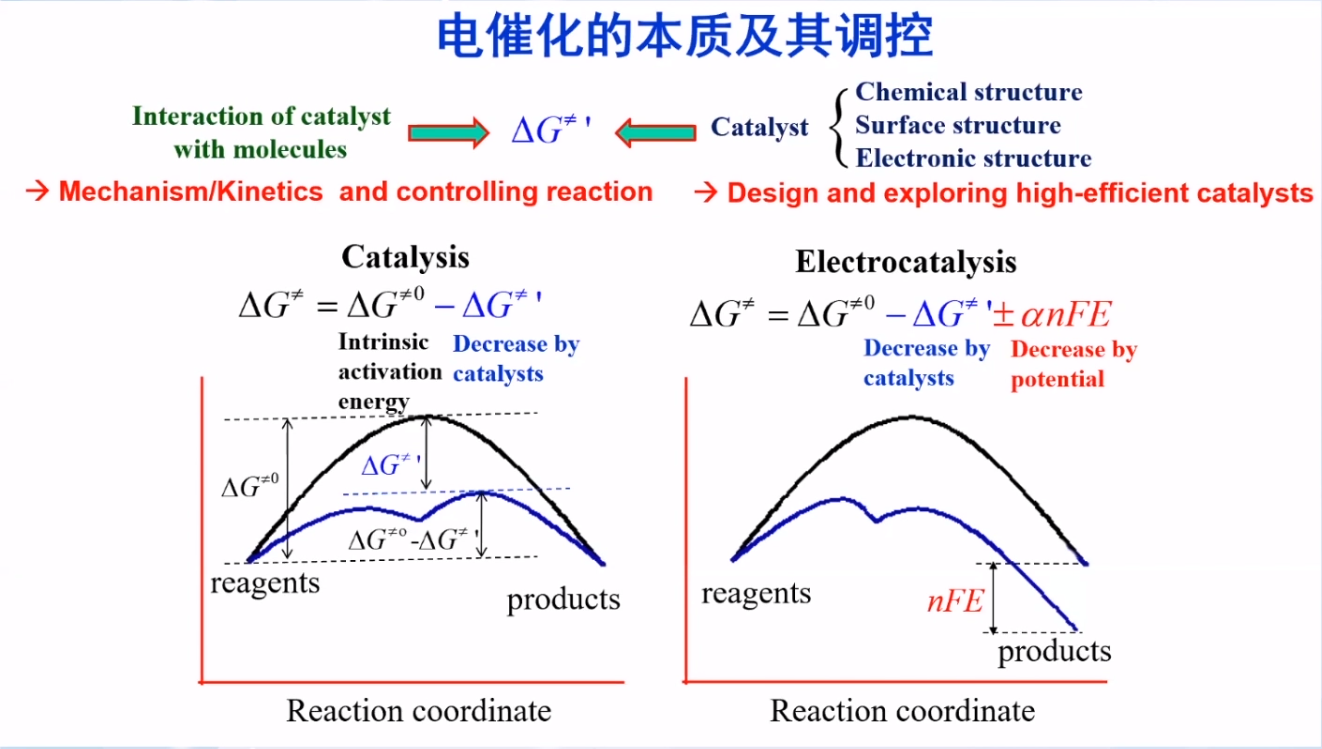
ΔG≠’描述的是催化剂的加入使反应的本征能垒降低的程度;主要由反应分子与催化剂表面的相互作用、催化剂结构(化学、表面、电子)等因素决定。
因此,调变催化剂性能,即增大ΔG≠’有两种途径:
1、从电催化机理入手,调控反应途径;
2、调控催化剂结构。
二、电催化机理和反应途径调控
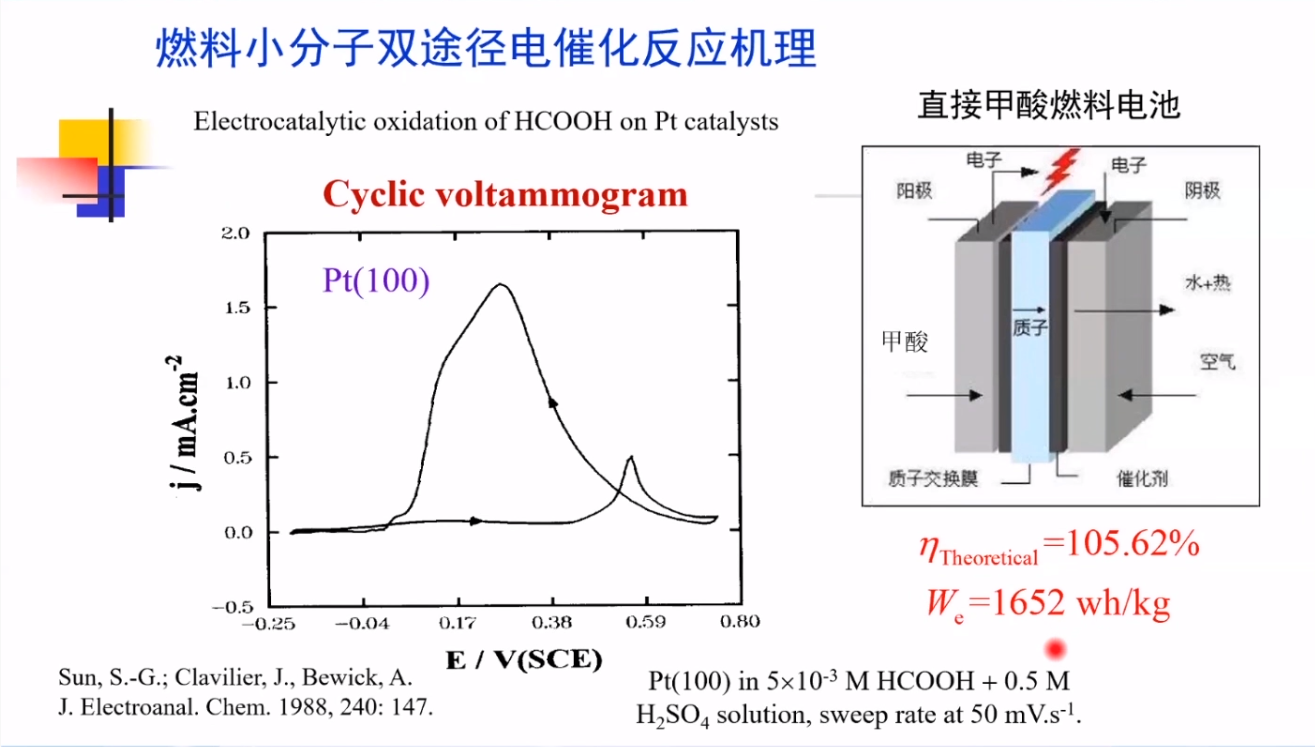
直接甲酸燃料电池CV曲线中正向扫描无电流、负向扫描大电流的原因:
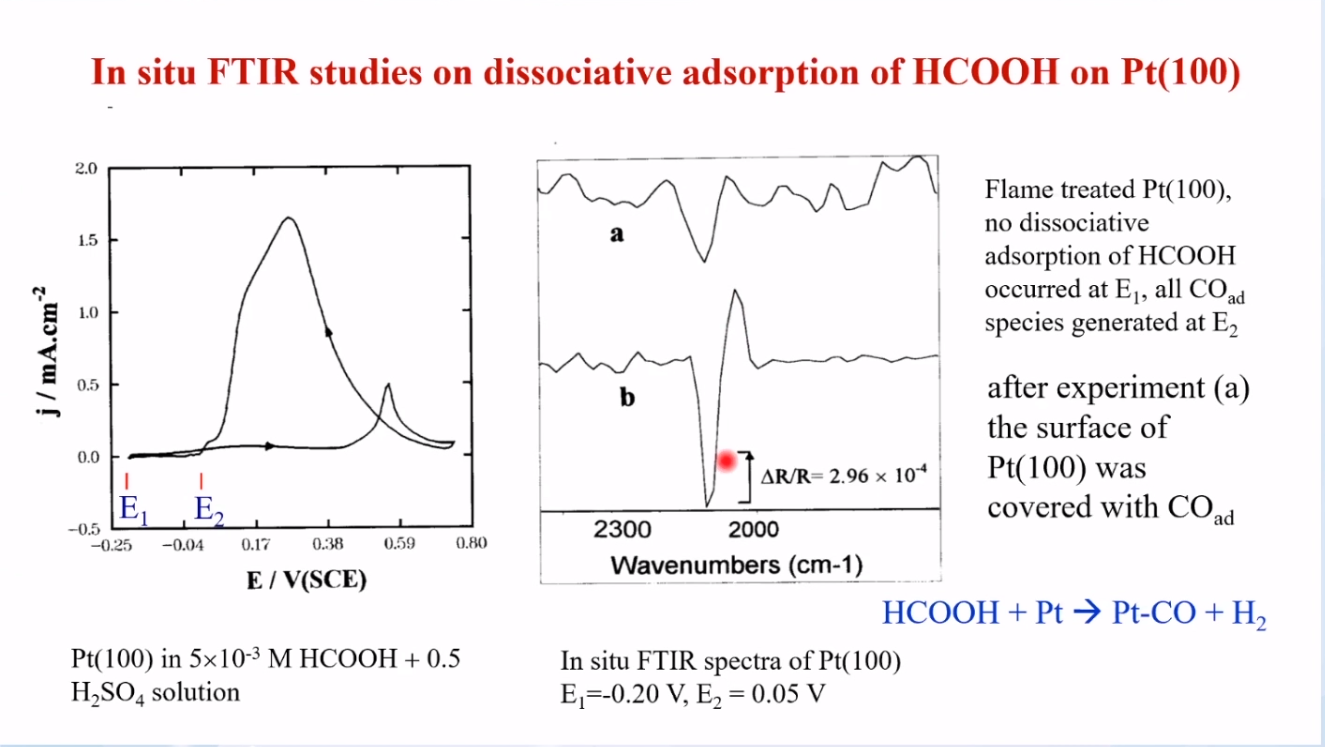
原位红外光谱发现,E1→E2电位下,Pt表面检测到CO。这是由于HCOOH在Pt表面上通过相互作用被解离生成CO和H2,CO吸附在Pt表面,Pt被毒化。因此,只有高电位下CO被除去后才呈现高氧化活性,出现大电流。
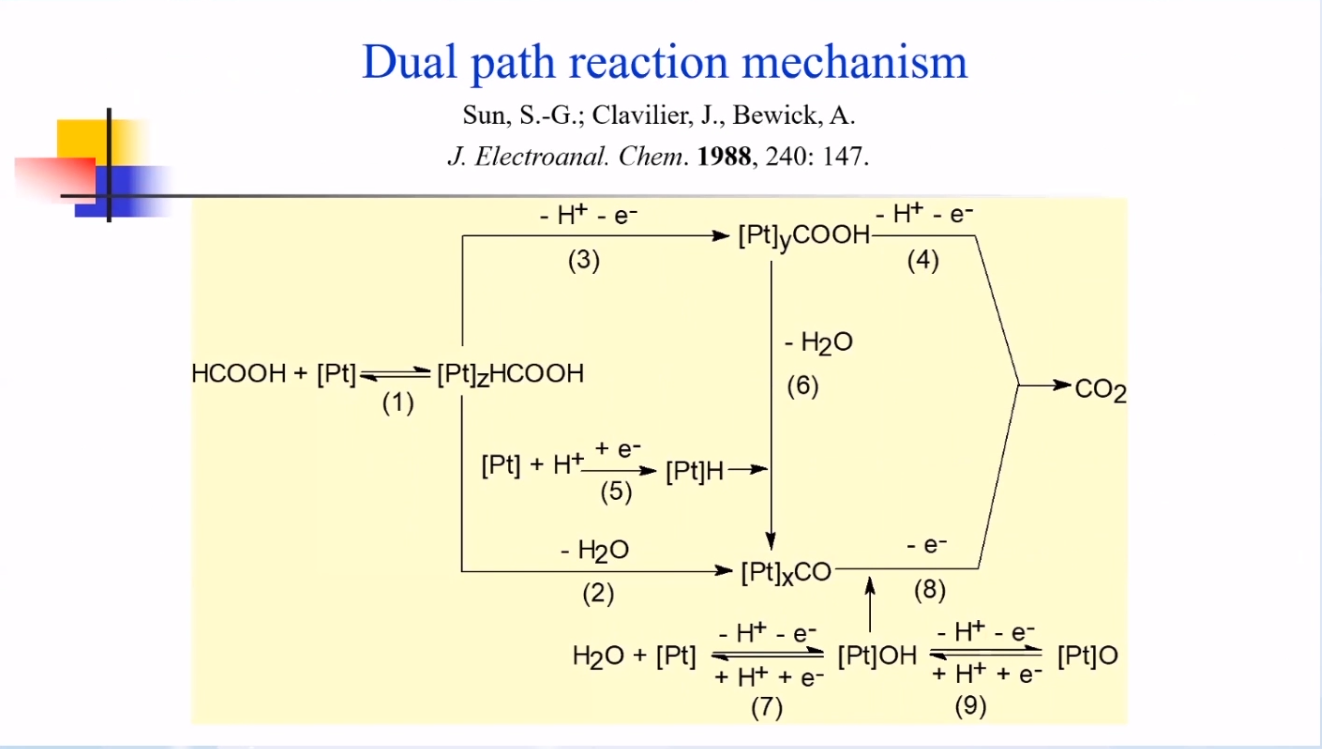
双途径反应机理:实际反应途径取决于于电极的表面结构。
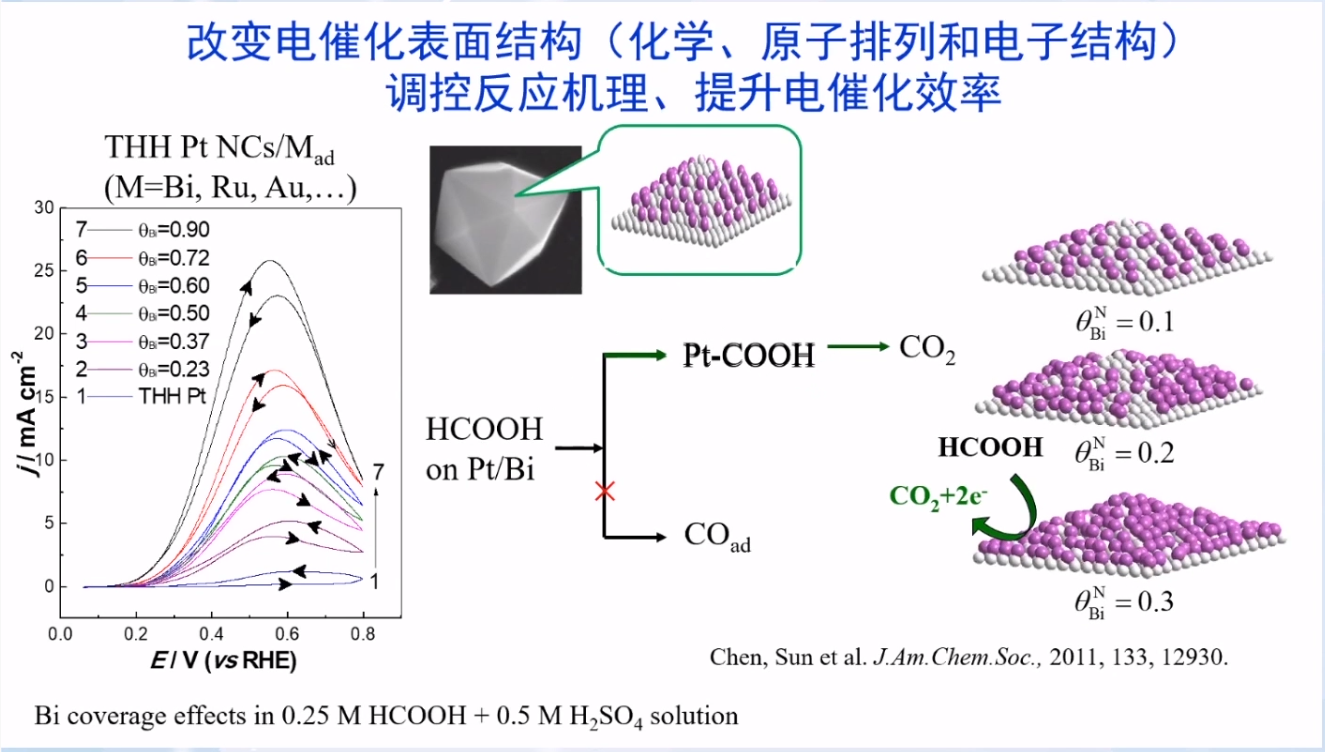
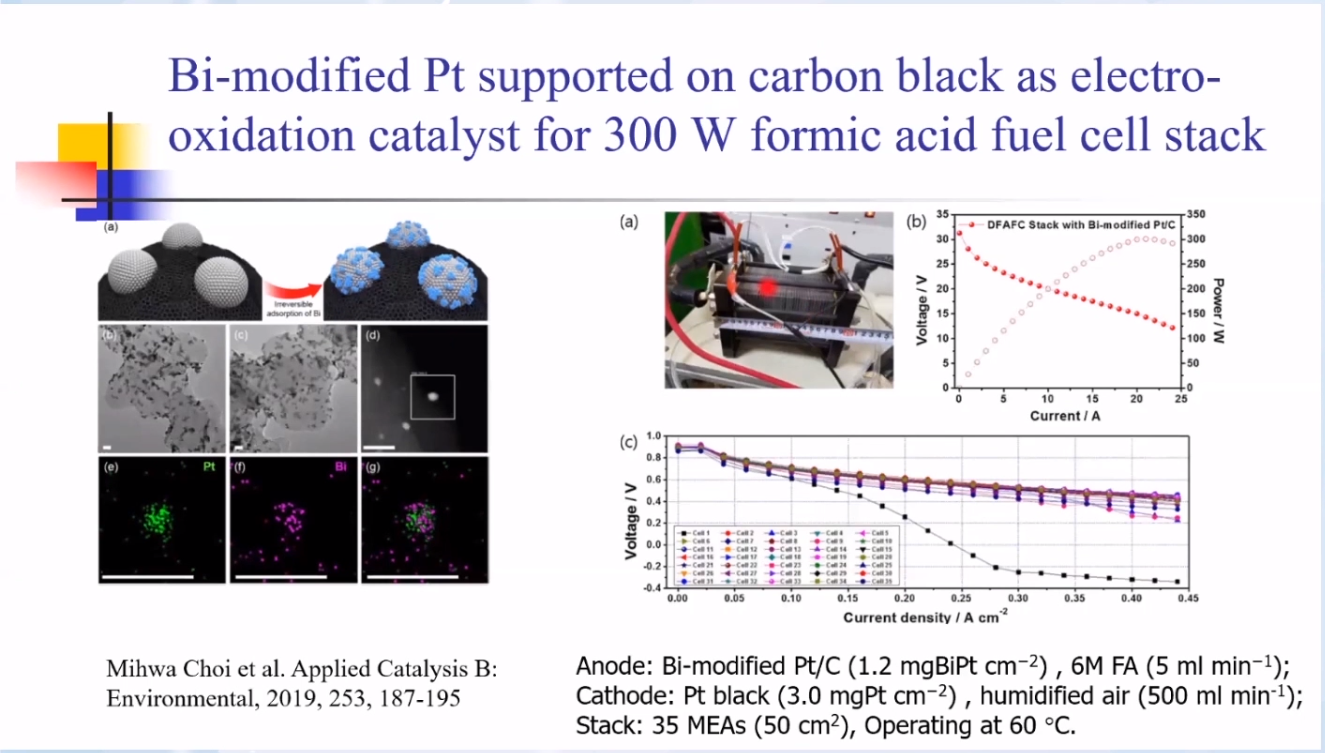
可通过改变电催化表面结构(化学、原子排列和电子结构)调控反应机理、提升电催化效率。
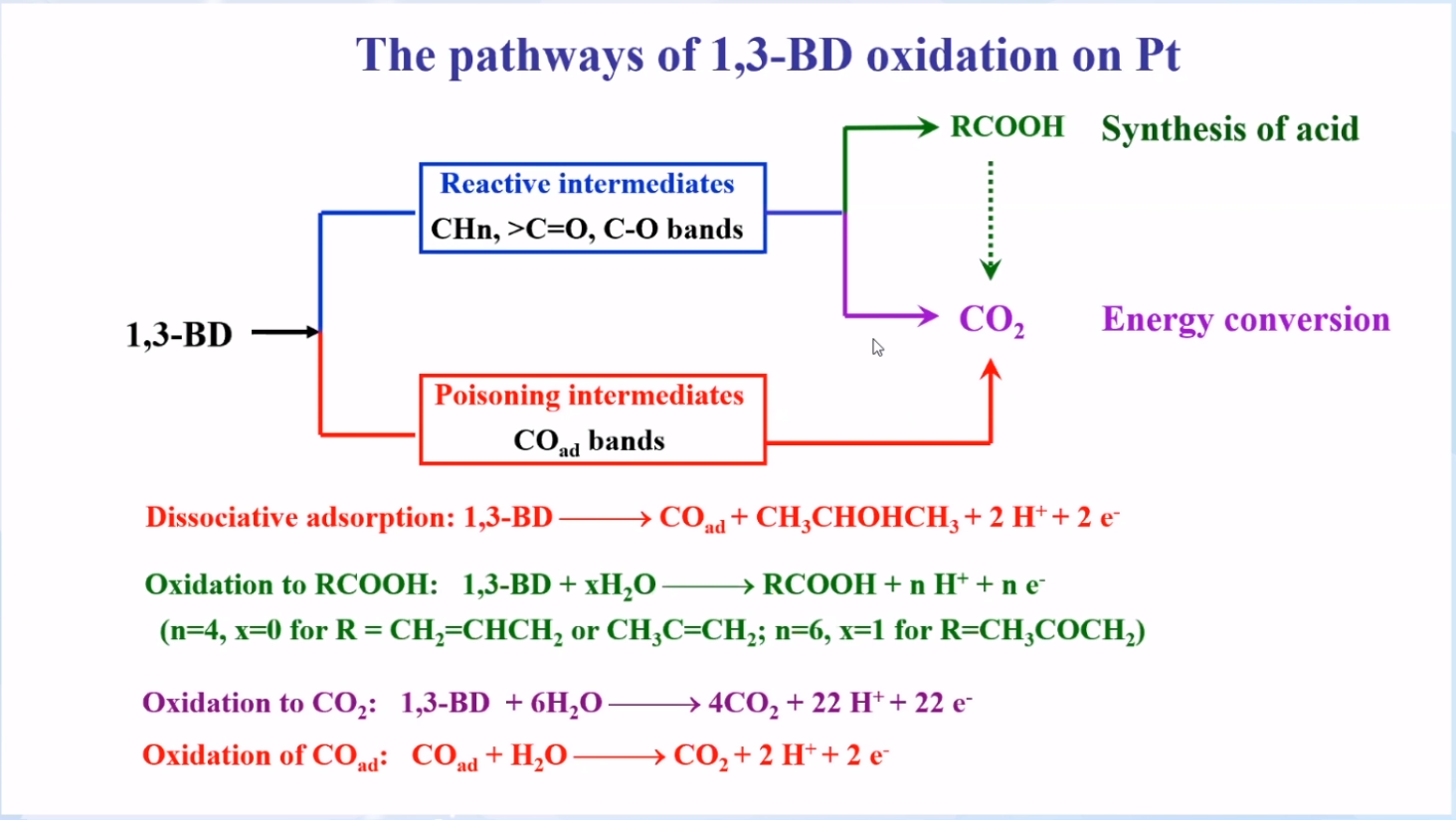
更复杂一点的例子是1,3-BD的电氧化:
途径一:解离吸附生成CO;
途径二:活化氧化生成RCOOH。
阻止解离吸附途径,避免生成毒性中间产物CO,后续经过调控反应途径可分别实现电催化合成和能源转换。
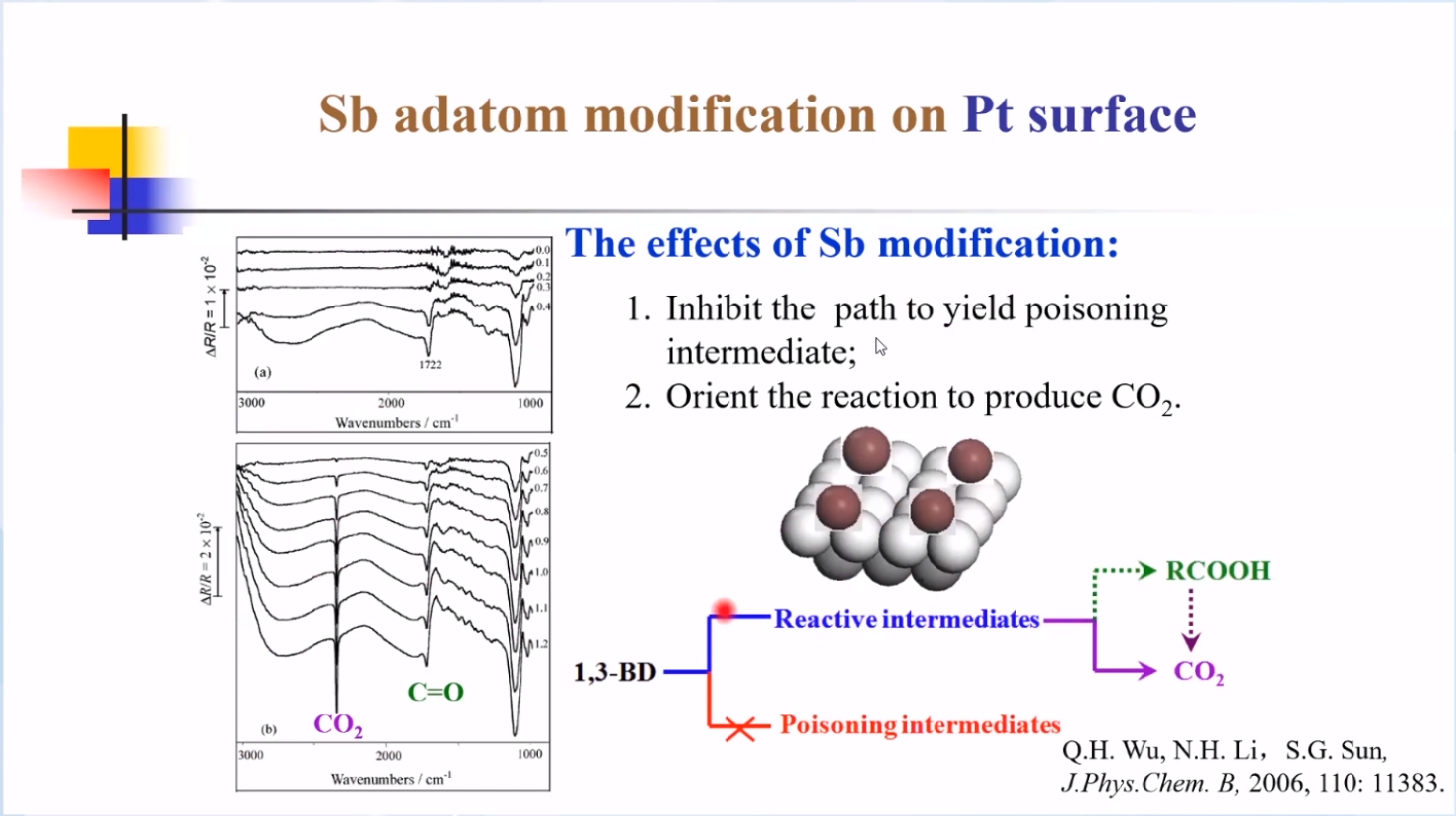
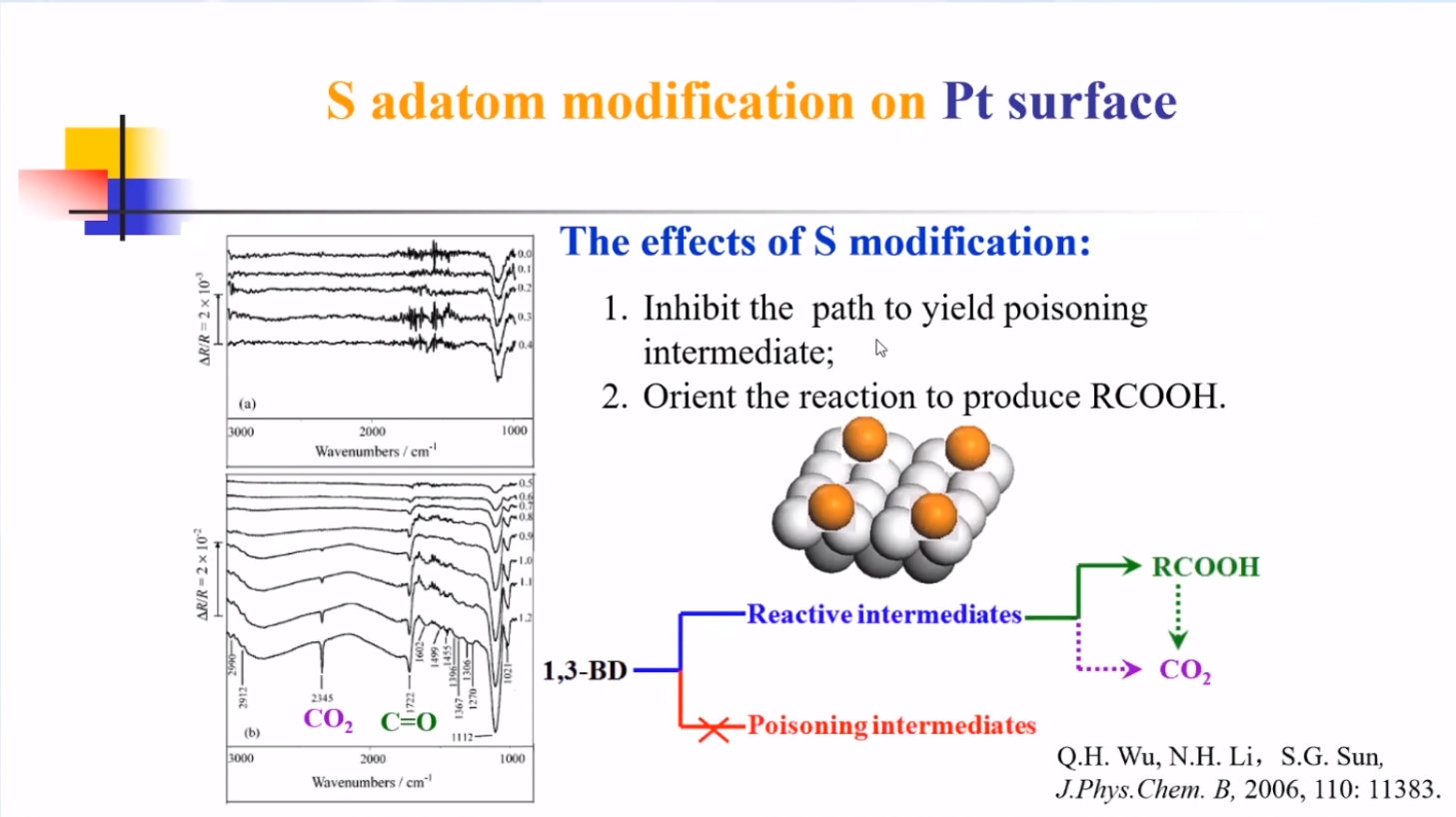
通过在Pt表面修饰Sb,反应产物主要为CO2,即可实现1,3-BD作为能源转换装置。
通过在Pt表面修饰S,反应产物主要为RCOOH,即可定向实现酸的电催化合成。
三、电催化表面结构效应
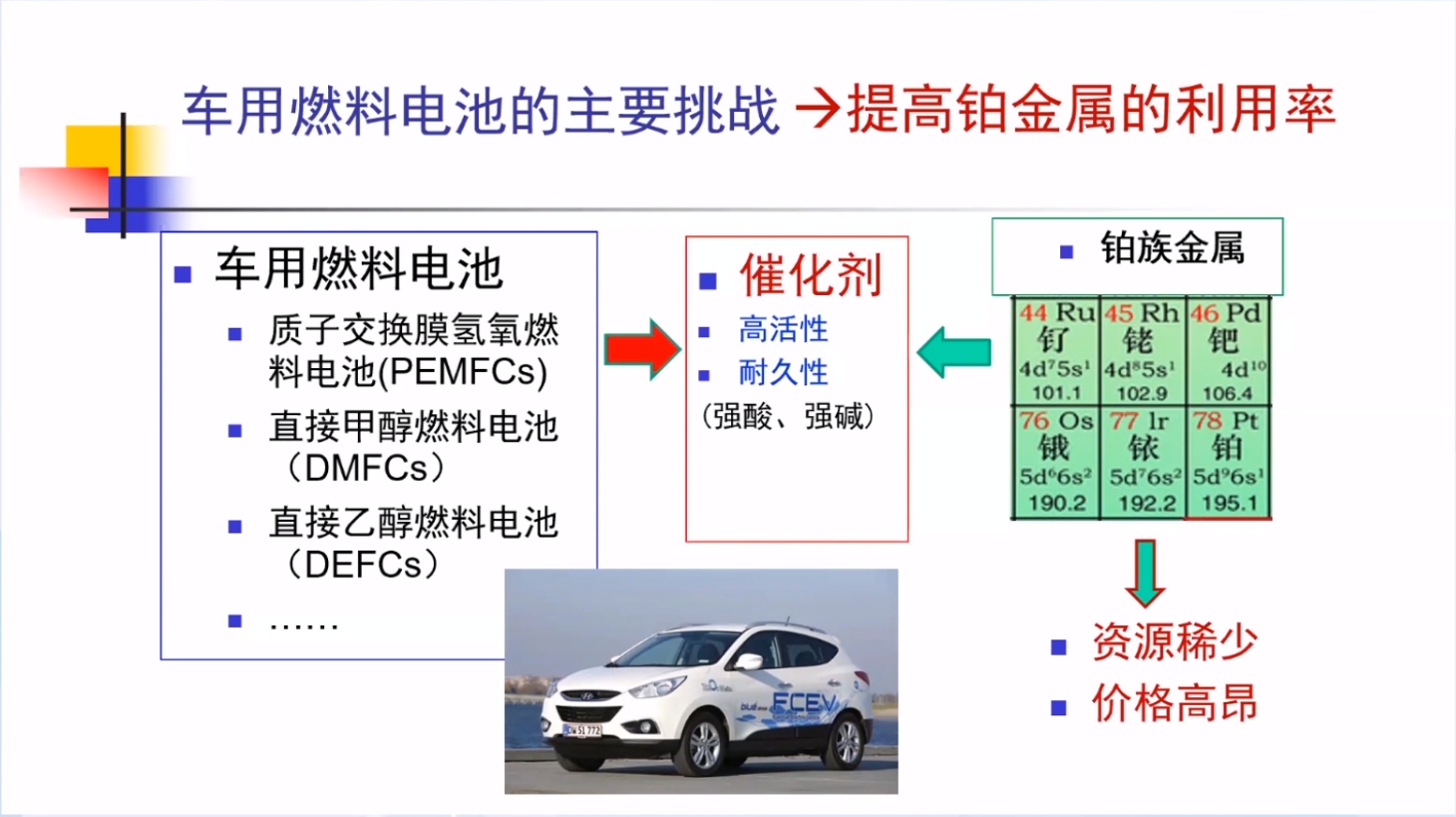
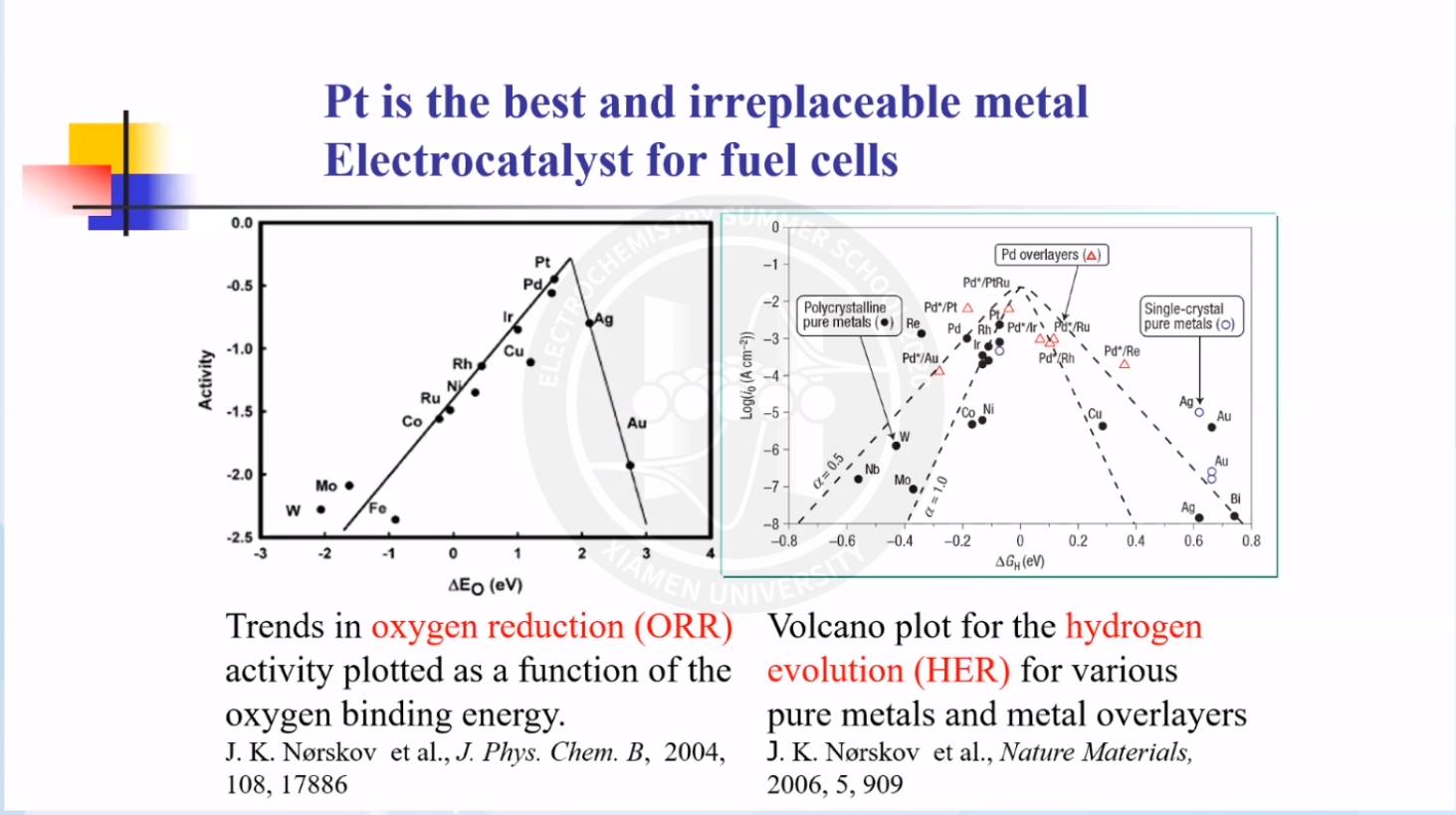

以车用燃料电池为例,适用的铂族金属催化剂具有资源稀少、价格高昂两大限制。因此,如何提高铂金属的利用率成为了车用燃料电池的主要挑战。
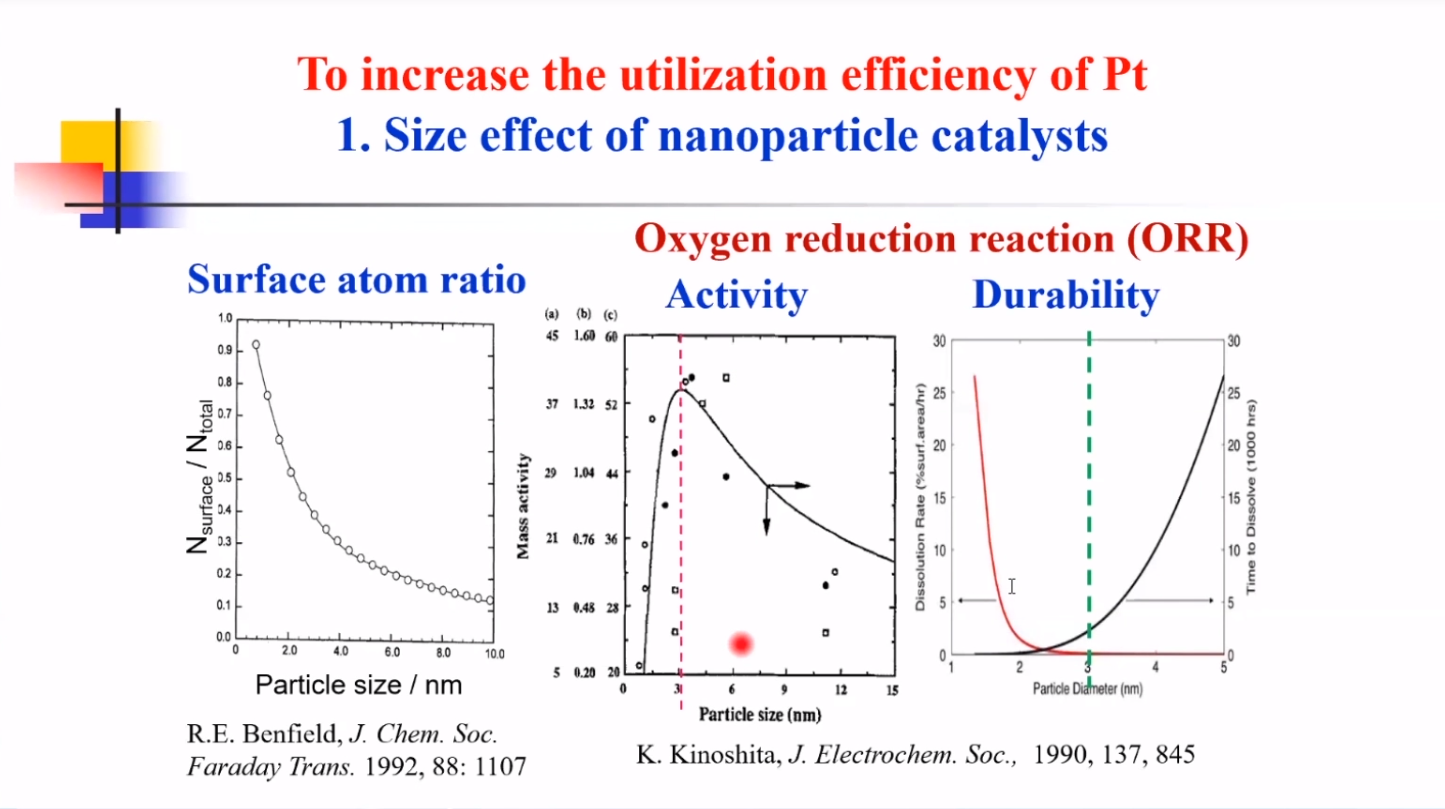
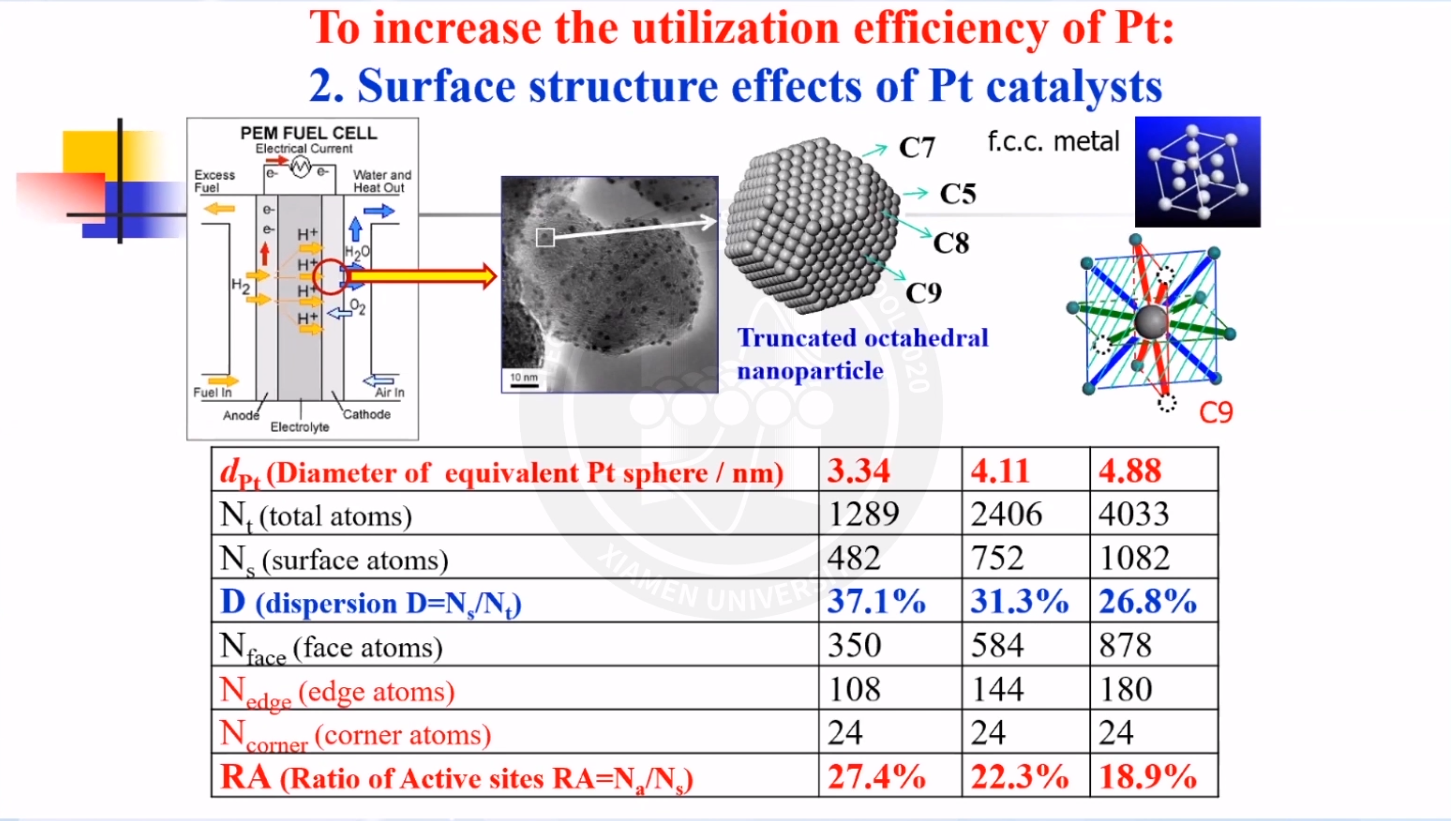
提高铂金属利用率的主要方式如下:
1、改变催化剂粒子的尺度:理论来说,随着催化剂粒子粒径的减小,比表面积增加,活性位点增多,催化剂活性逐步提高;但在实际反应过程中,过小的粒径(<3nm)会影响催化剂的稳定性,反而会降低催化活性。
2、改变催化剂表面结构:Pt原子配位数越低,催化活性越高。
(一)传统单晶模型催化剂
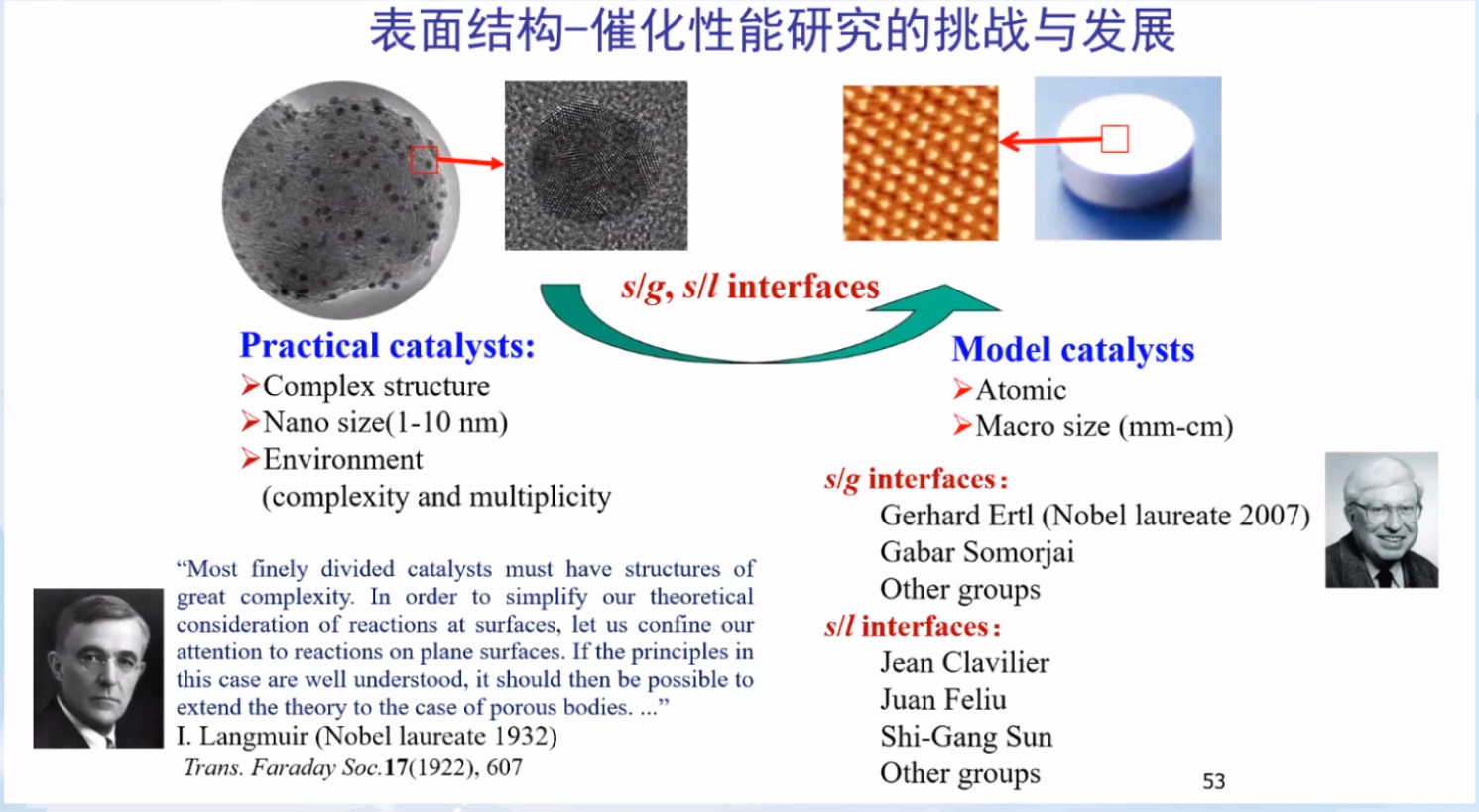
实际催化剂表面结构非常复杂,为了研究催化剂表面结构与催化性能关系,科学家们提出用表面原子结构排列明确的金属单晶面作为模型催化剂。
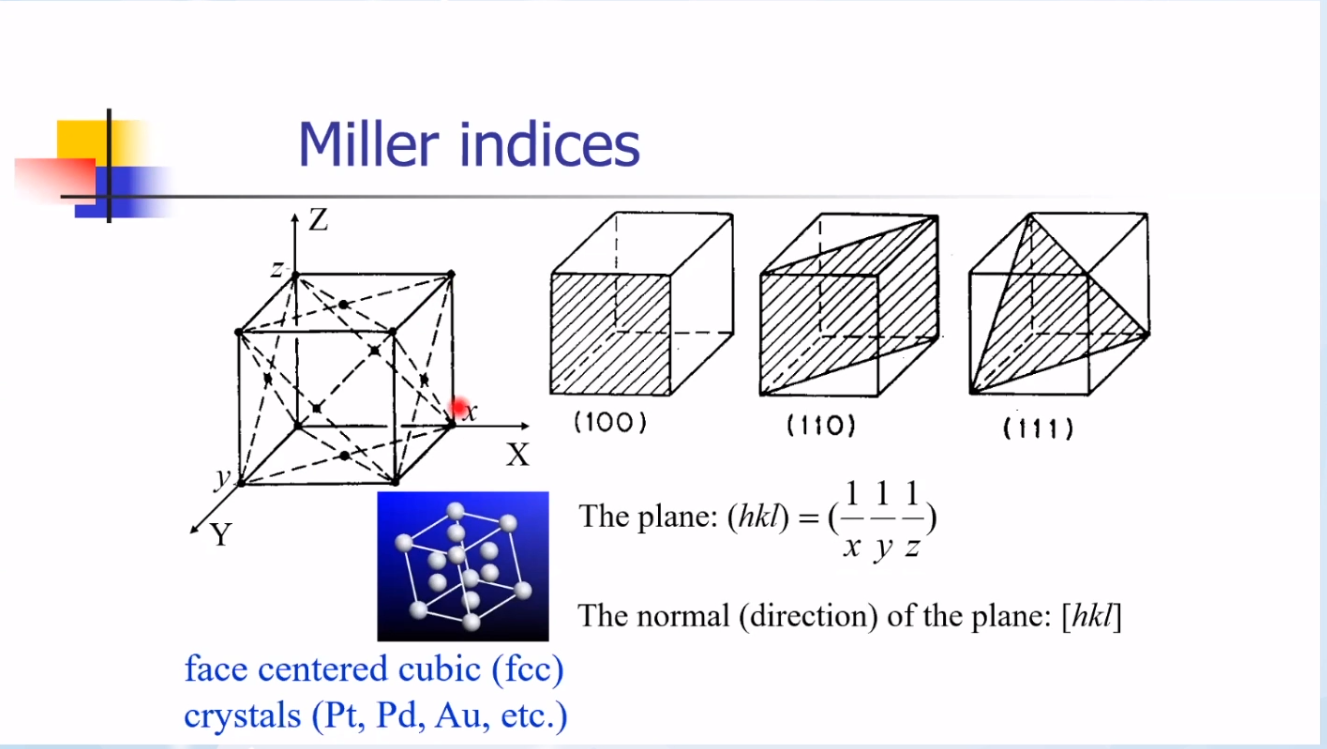
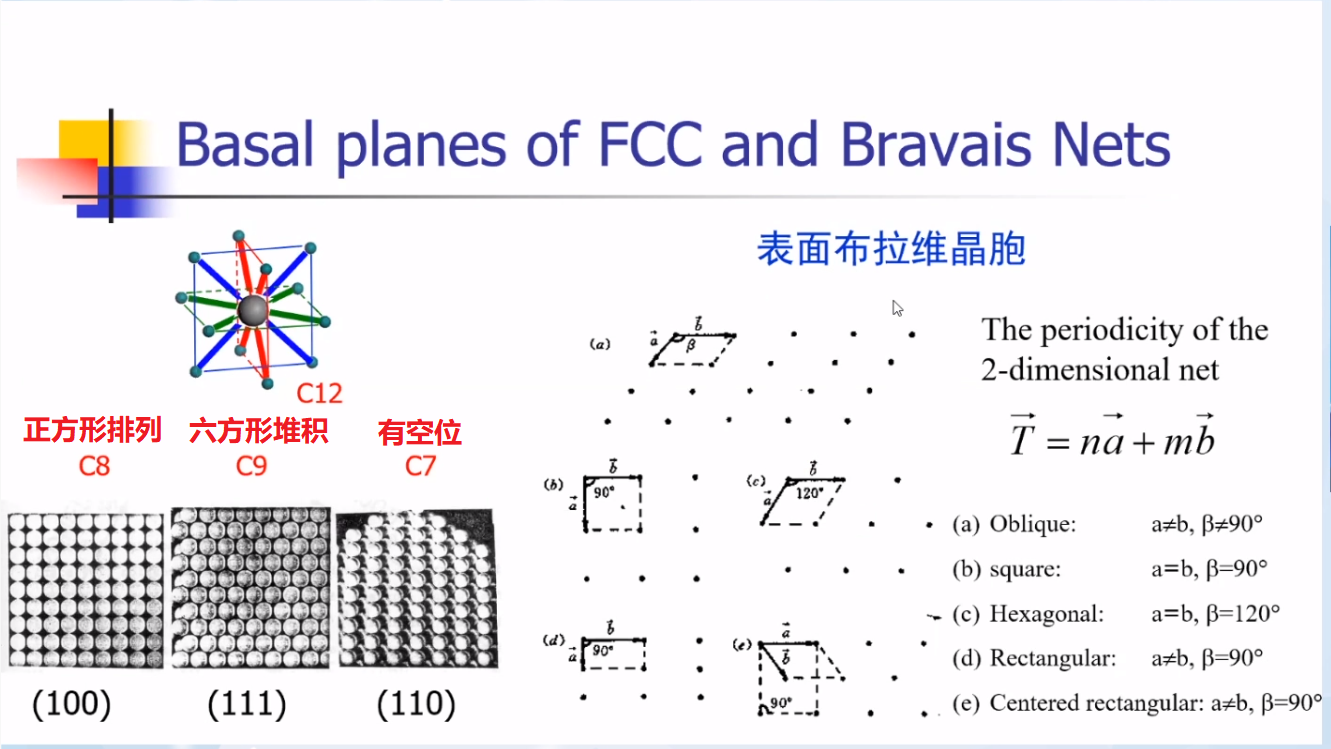
金属单晶面通常用米勒指数(晶面指数)来描述。不同晶面的结构不同,表层原子不同晶面的配位数不同。
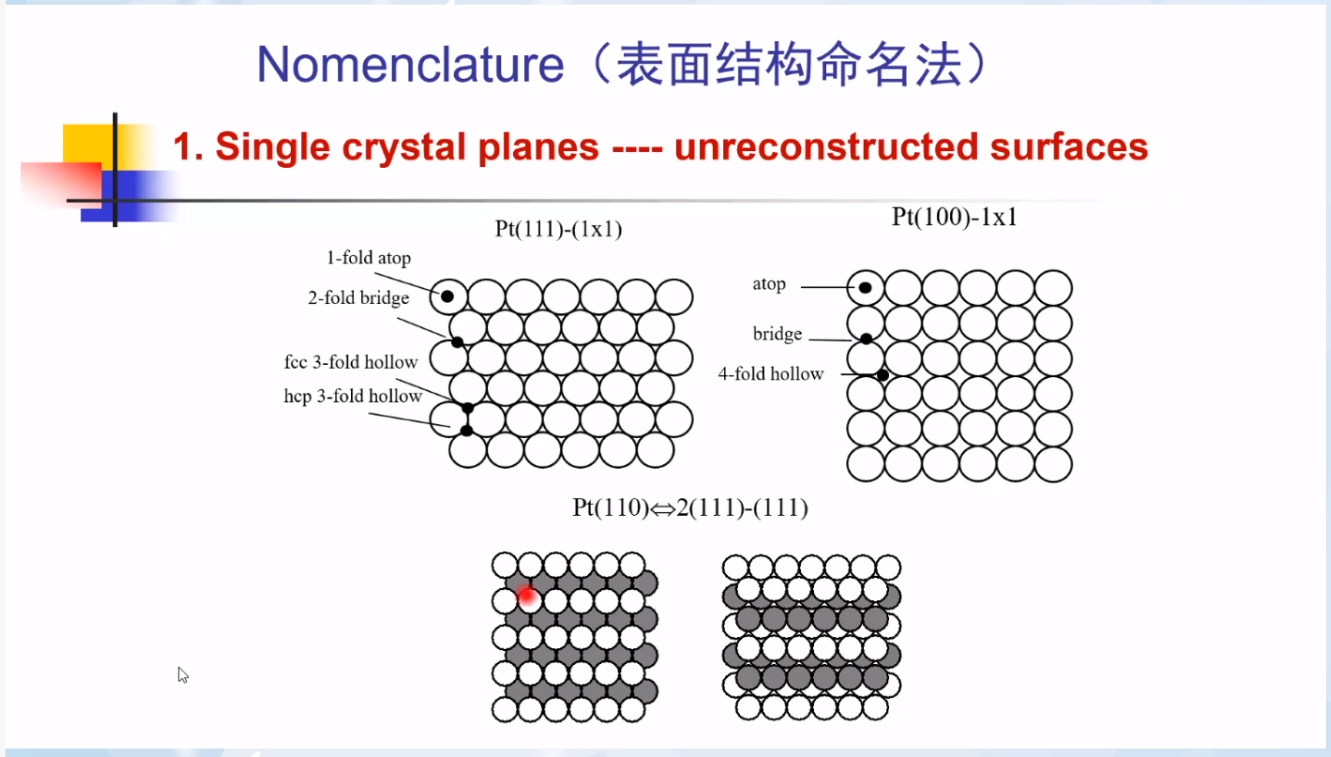
上图展示了(111)、(100)和(110)晶面的表面位点。不同结构、不同位点环境不同,反应性能不同,所以需要对表面结构进行更细致的分析。
表面结构分析:
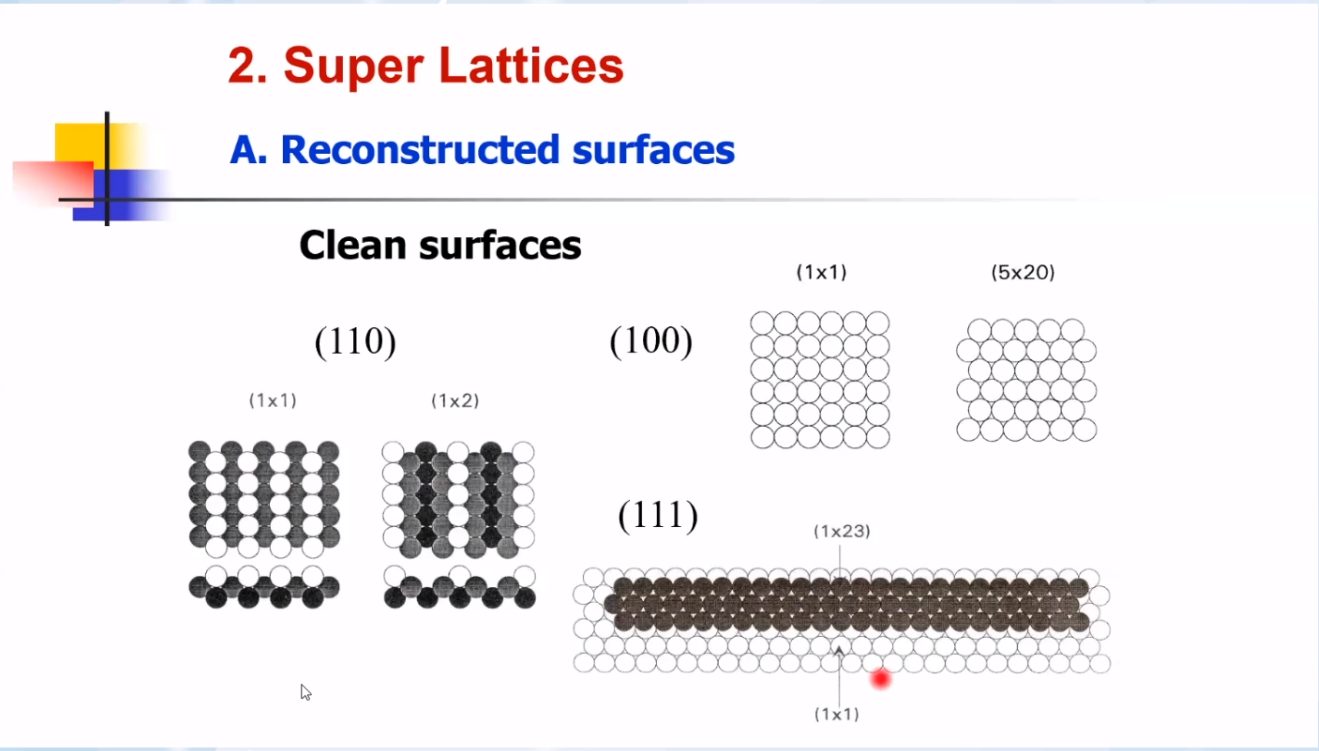
(1)本体结构:
① 表面晶面结构不发生重建,与体相晶面结构保持一致→(1╳1)
② 表面晶面结构发生重建,形成更紧密的原子排列结构,使体系能量更低→(1╳2)、(5╳20)、(1╳23)
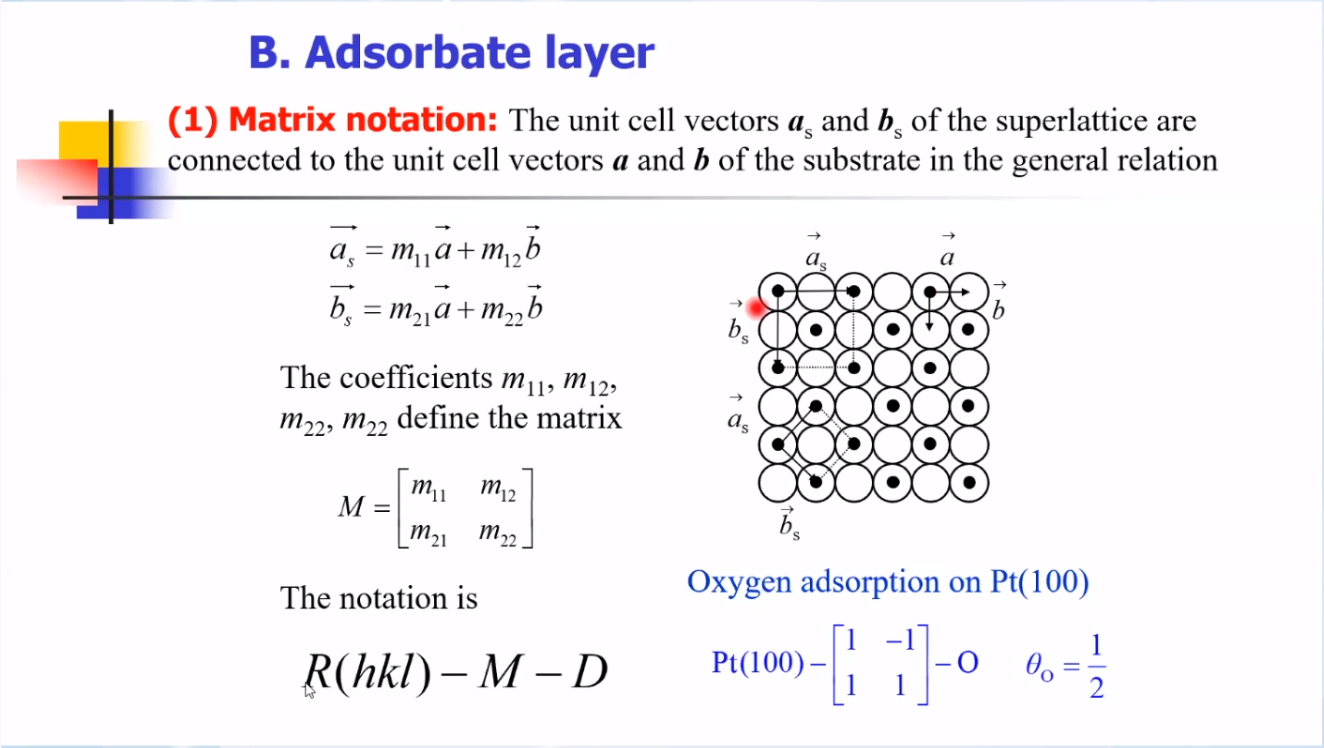
(2)吸附层结构:除了催化剂本体以外,表面会吸附其它分子。通常用以下两种方式表示:
① Matrix natation
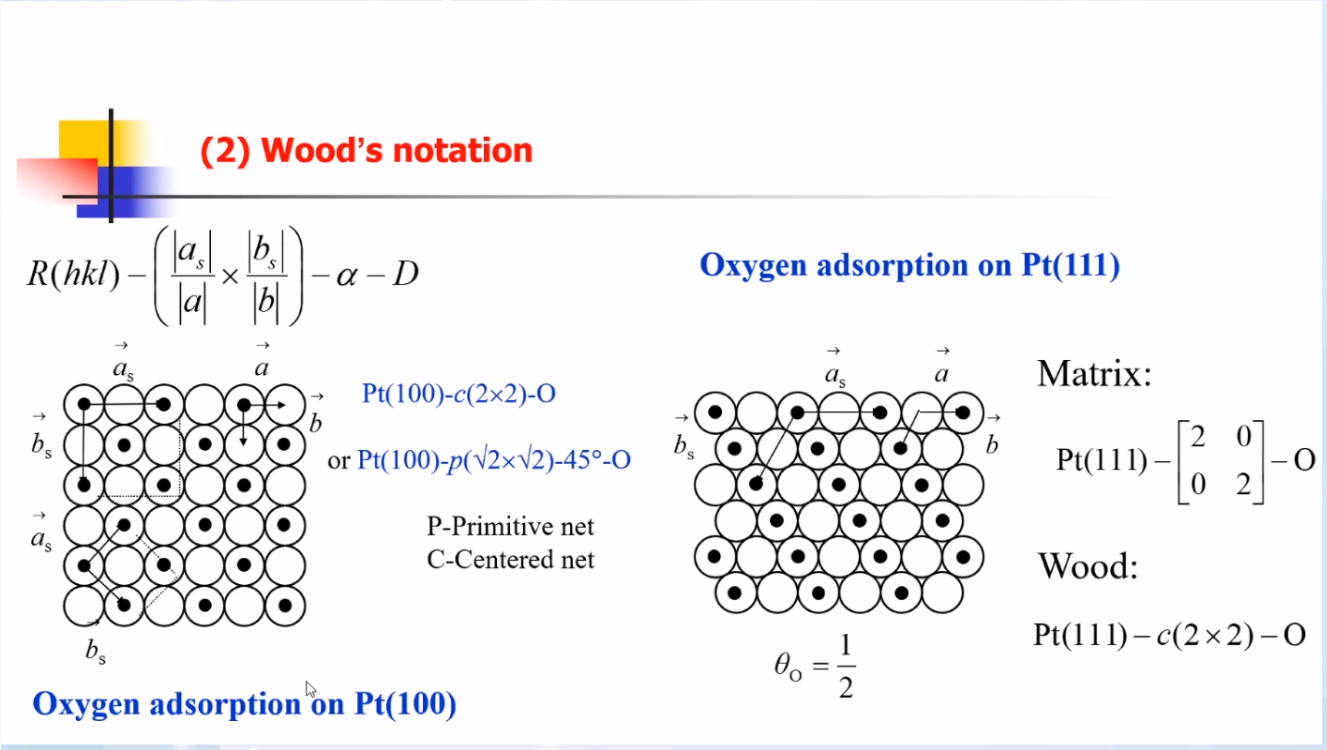
② Wood's natation
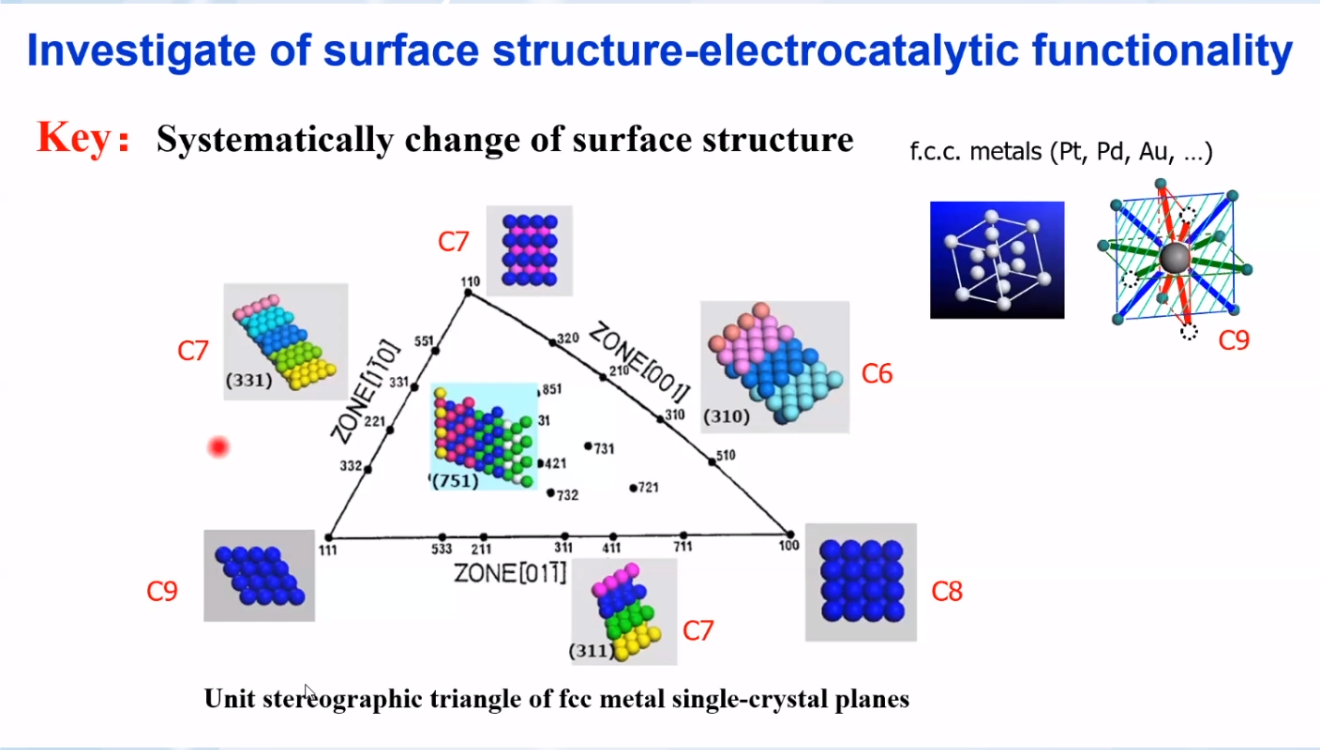
由上图所示,在三条晶带轴上的高指数晶面都平行于晶带轴,且表面原子配位数较低;在三个顶点上的低指数晶面的表面原子配位数较高。即高指数晶面的催化活性比低指数晶面的催化活性更高。
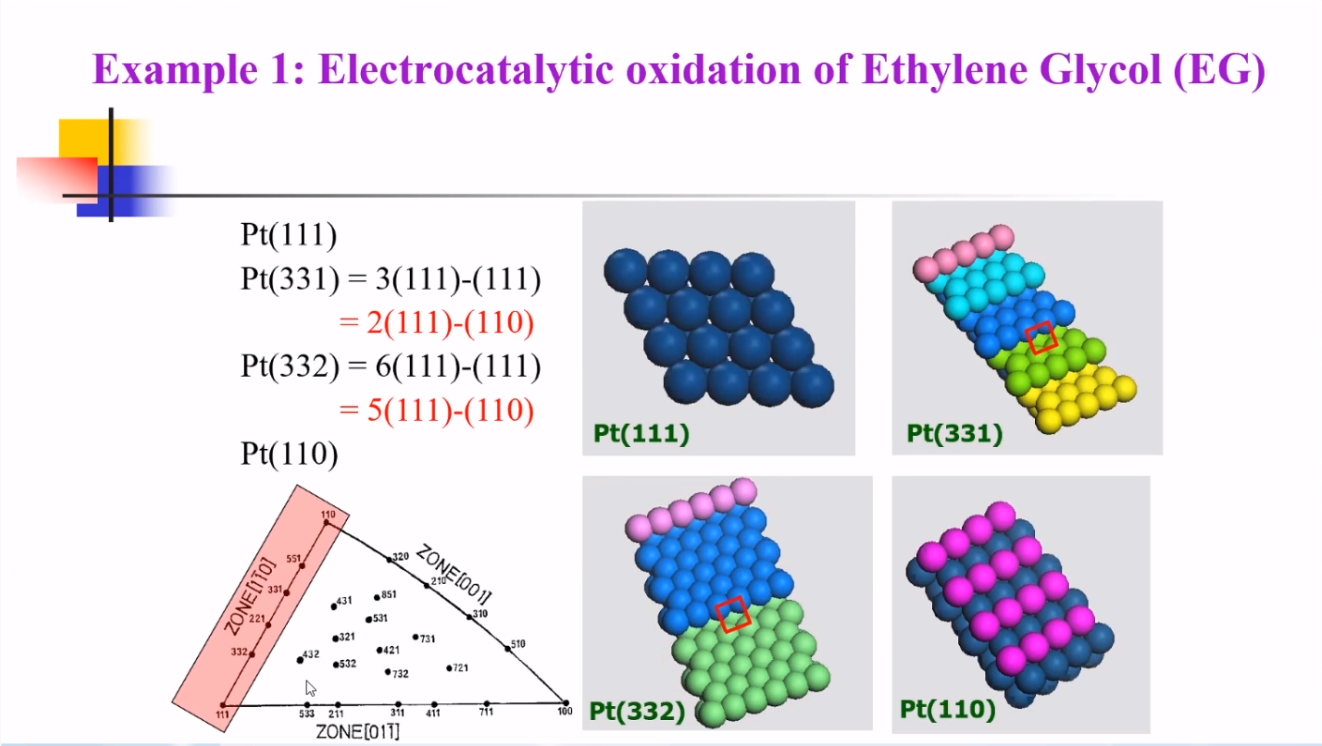
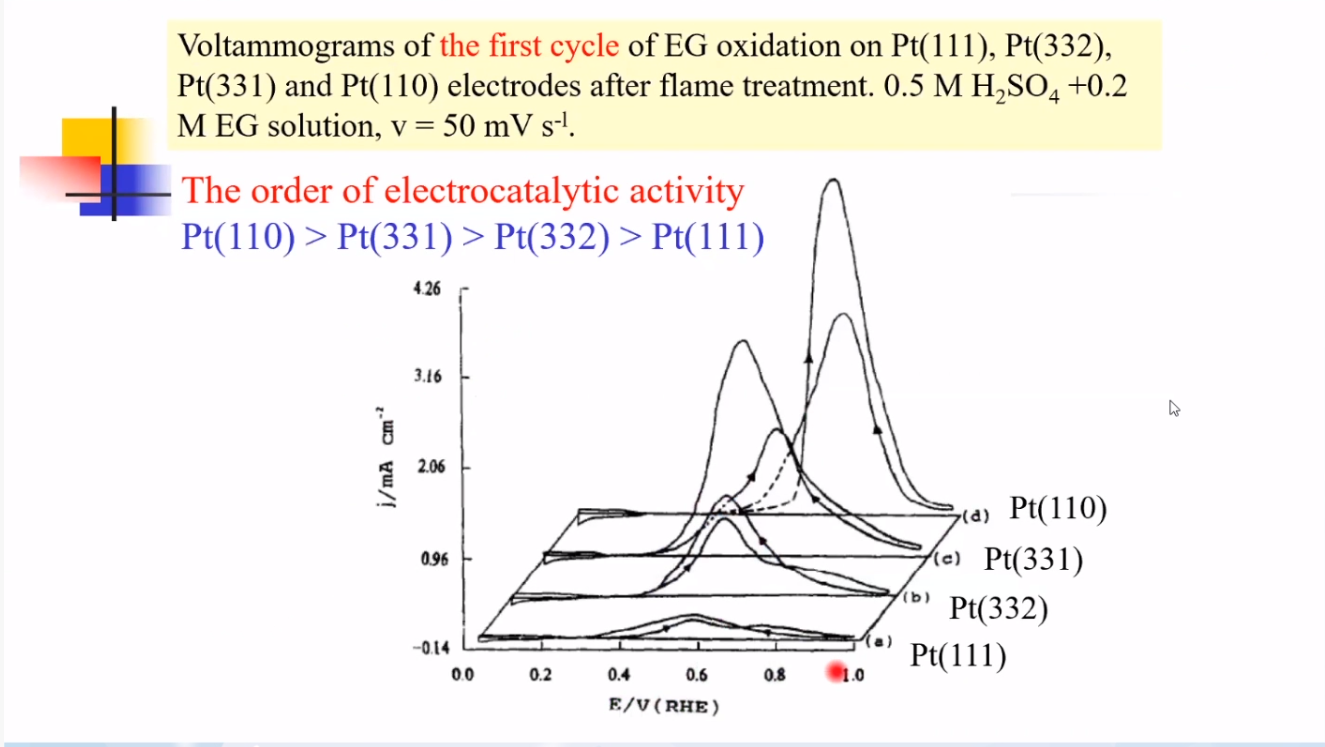
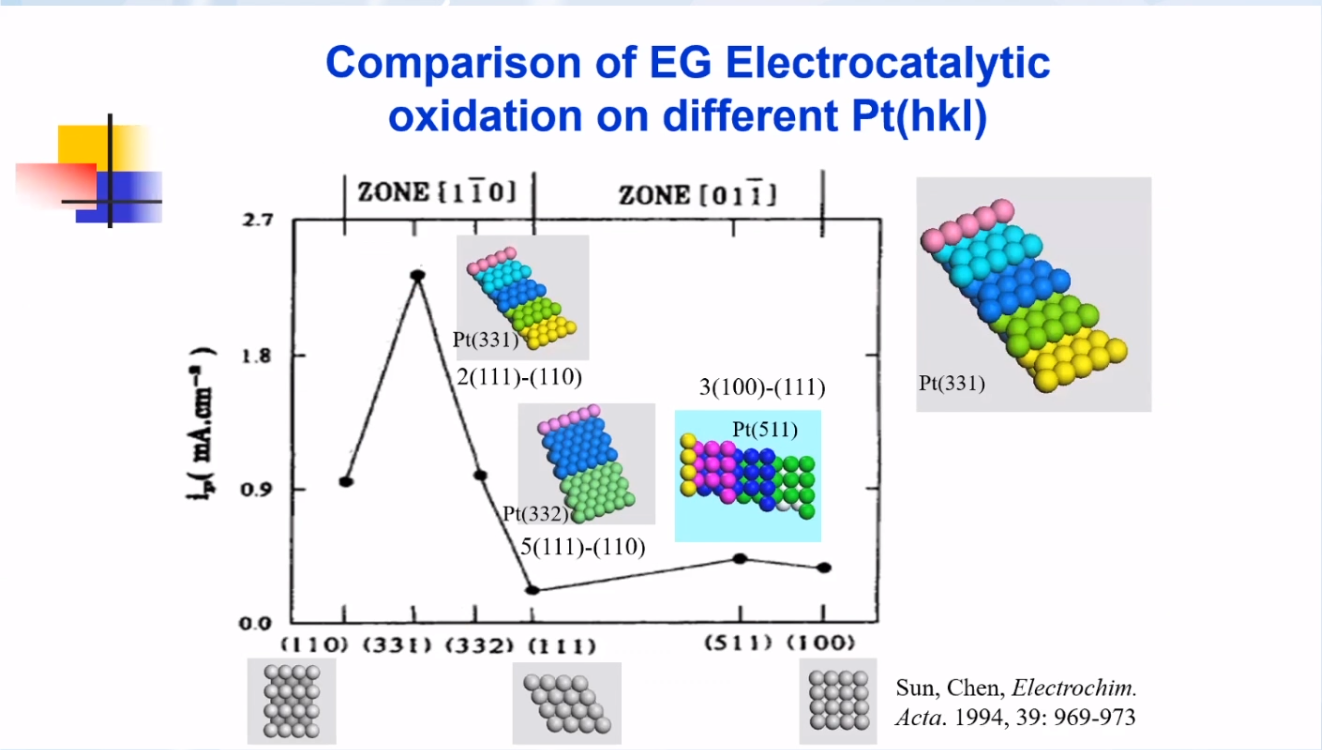
以乙二醇的氧化过程为例,根据CV图中的峰电流值大小可以确定不同晶面的电催化活性大小。
初始状态:
Pt(110)>Pt(331)>Pt(332)>Pt(111)
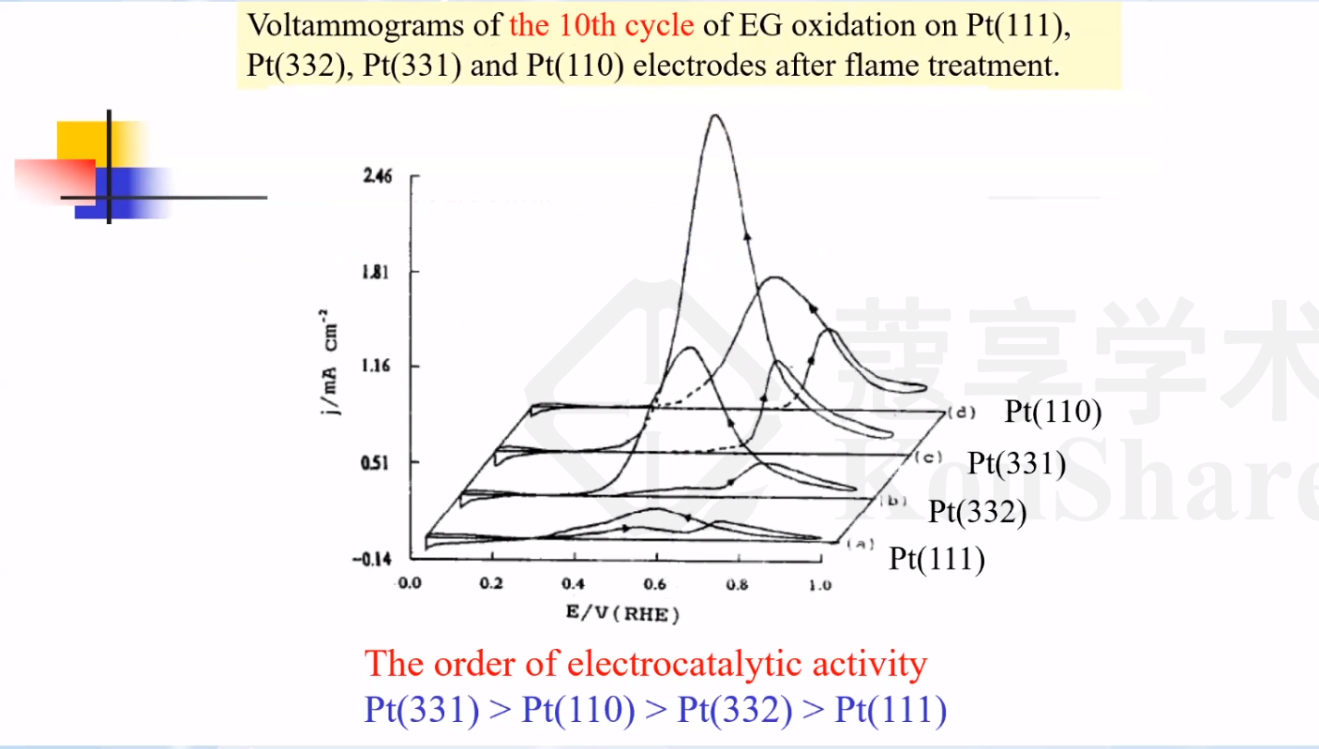
长期循环后:
Pt(331)>Pt(110)>Pt(332)>Pt(111)
表明在反应过程中,晶面的活性和稳定性会发生变化。Pt(331)晶面既具有高活性,又具有高稳定性。
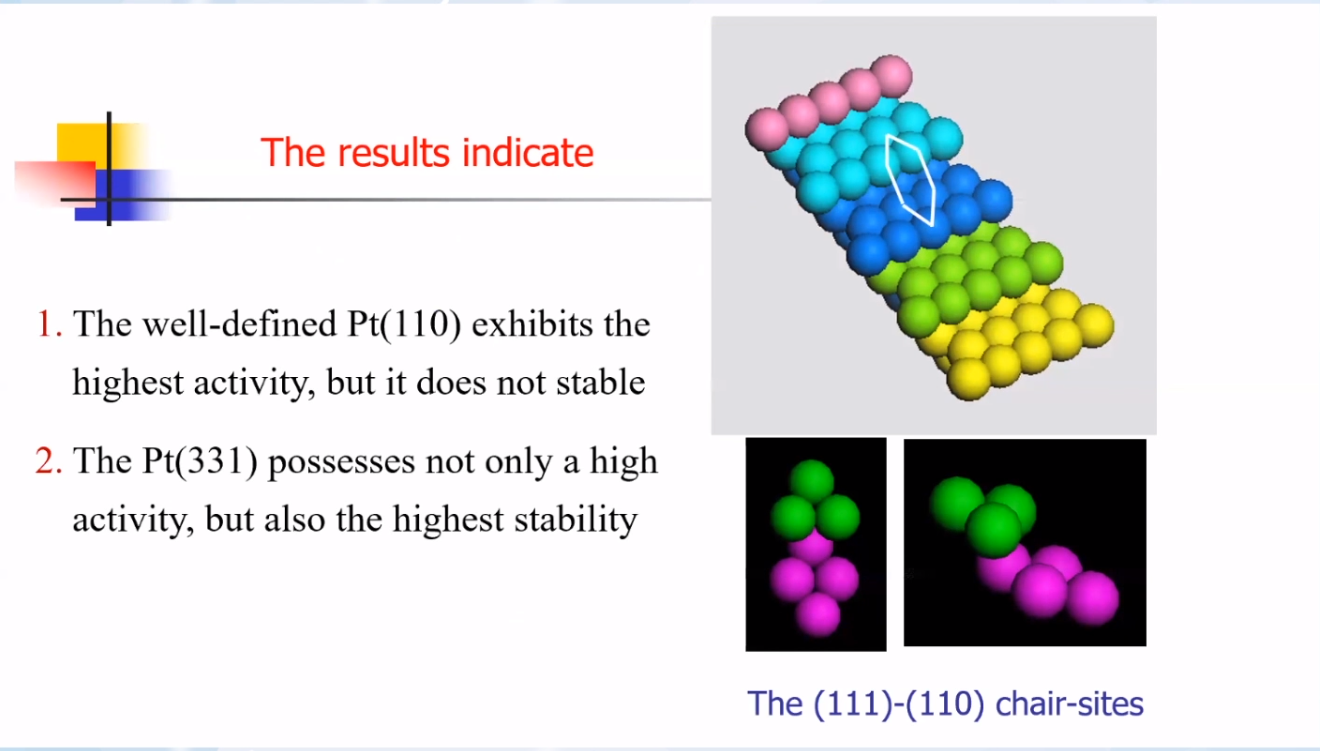
因为Pt(331)表面上形成了(111)–(110)椅式台阶位,该立体位点既有高活性,又有高稳定性。

活性中心是由5–6个低配位的原子组成,同时形成了一定的立体结构,如椅式结构Pt(310)、折叠五边形结构Pt(320)。
高活性表面含有高密度的活性中心,且作为开放性表面具有很高的表面能。
活性中心的概念可用于指导实际催化剂的设计。若纳米催化剂的表面结构都是由活性中心组成,其活性将大幅提升。
(二)二十四面体纳米晶Pt催化剂
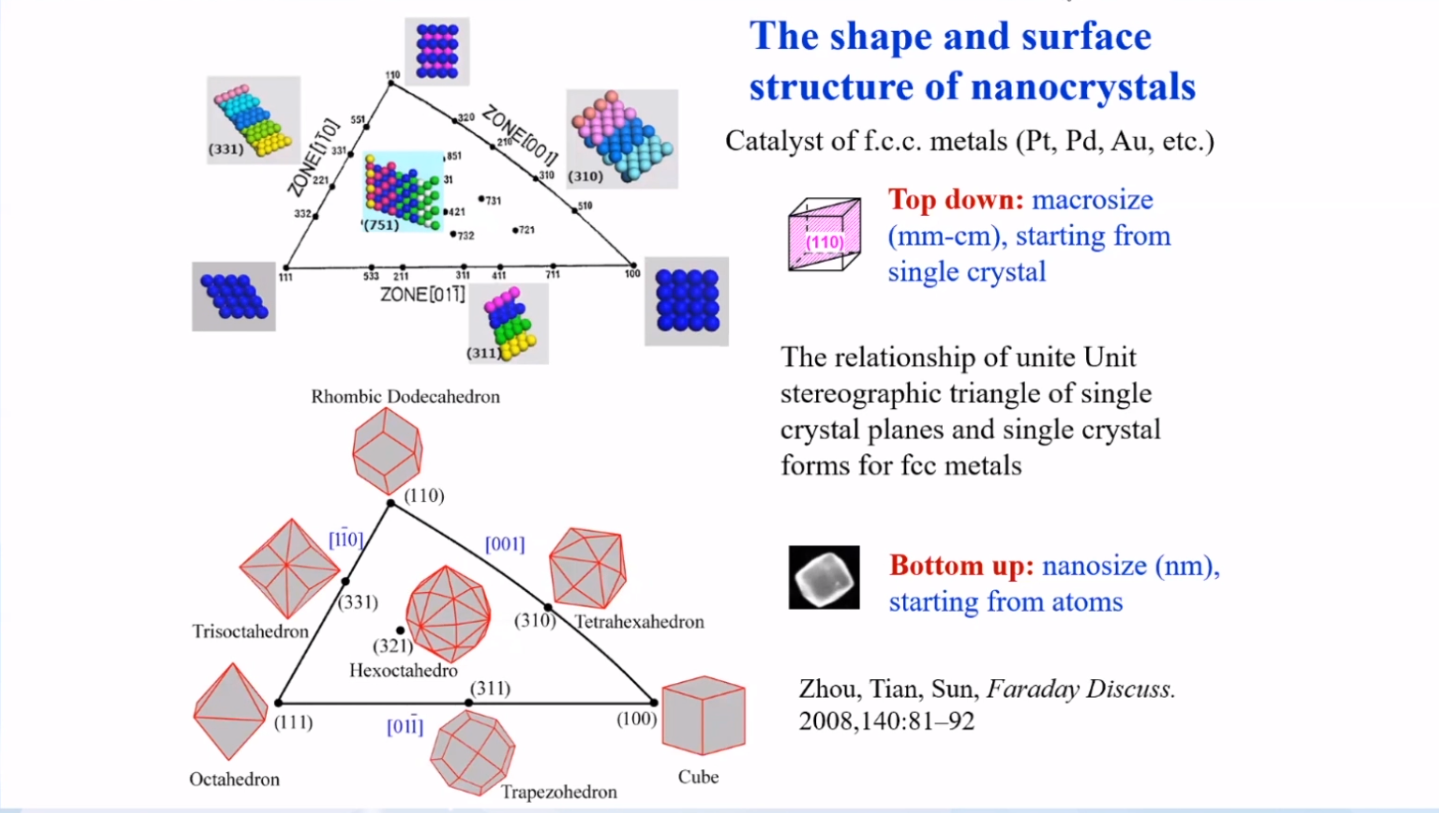
纳米晶的形状与其表面原子排列结构存在对应关系。上图展示了面心立方晶系(fcc)金属晶体表面原子排列与其形状(正立方体、八面体、菱形十二面题、五角十二面体、四角三八面体、四面体、六面体与八面体聚形)的相关关系。因此 ,通过纳米晶的形貌控制合成就可以调控催化剂的表面原子排列结构。

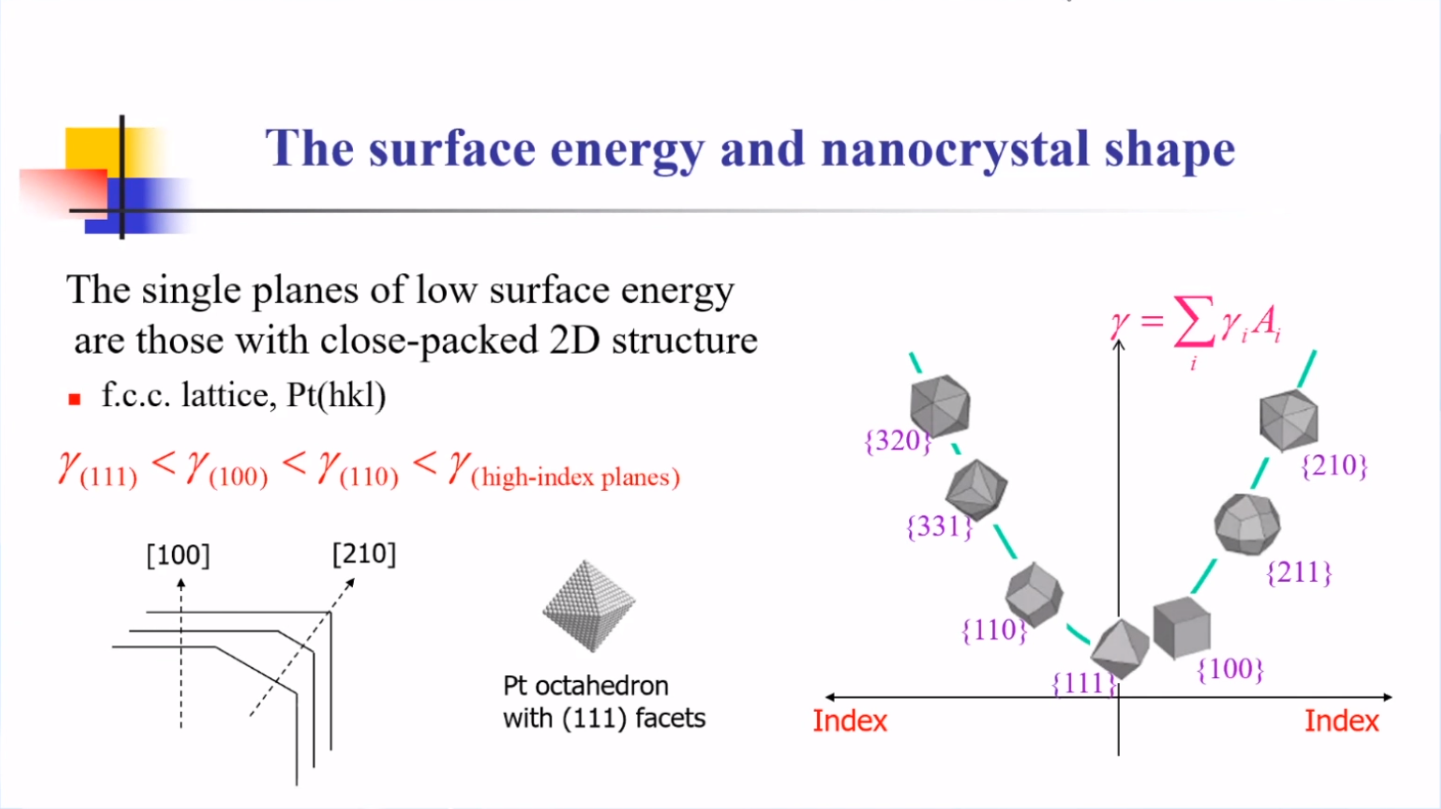
晶体结晶的热力学分析:
1、化学势/电化学势驱动使晶体生长;
2、表面能最低的晶体表面最易生成。
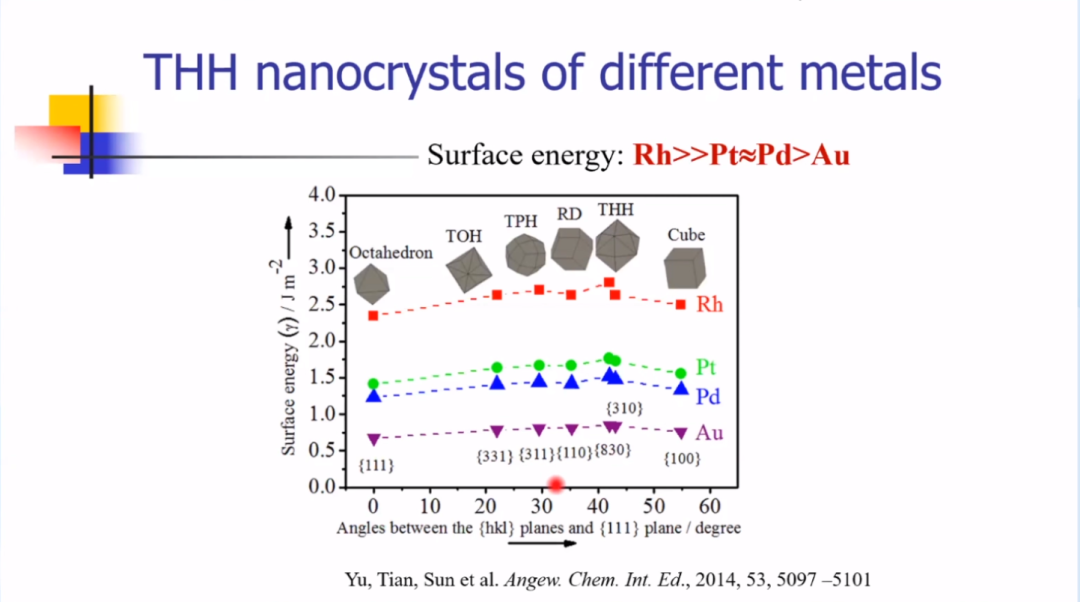
上图为不同形貌的贵金属纳米晶和相应晶面表面能的变化趋势:
(1)Au、Ag等金属表面能相对较低,可通过化学法合成高指数晶面结构的纳米晶(通常需要在溶液中加入表面活性剂、聚合物、小分子或离子等添加剂)。
(2)Rh、Pt和Pd等金属表面能相对较高,其高指数晶面结构的纳米晶的合成由于热力学限制仅依靠化学法几乎是无法实现。

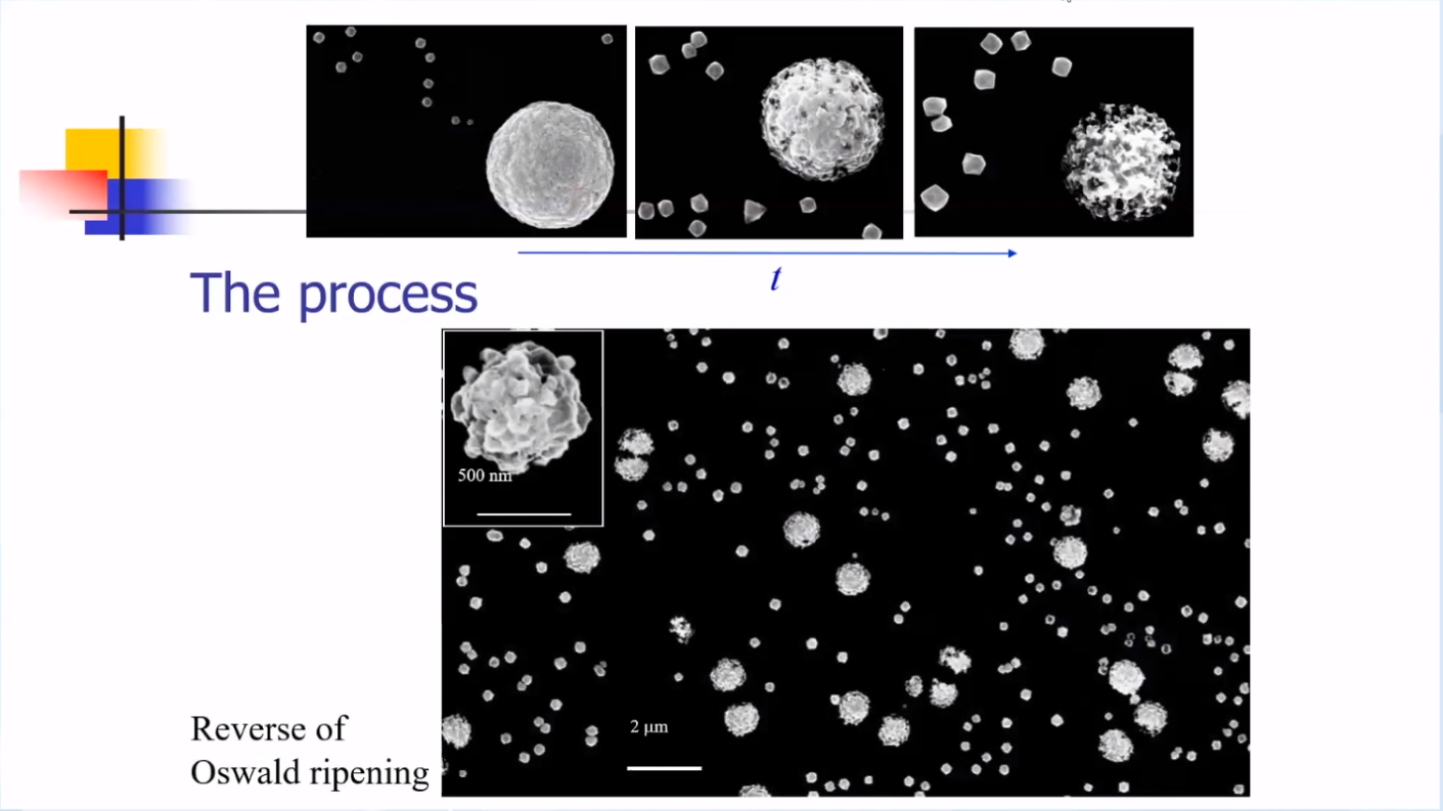
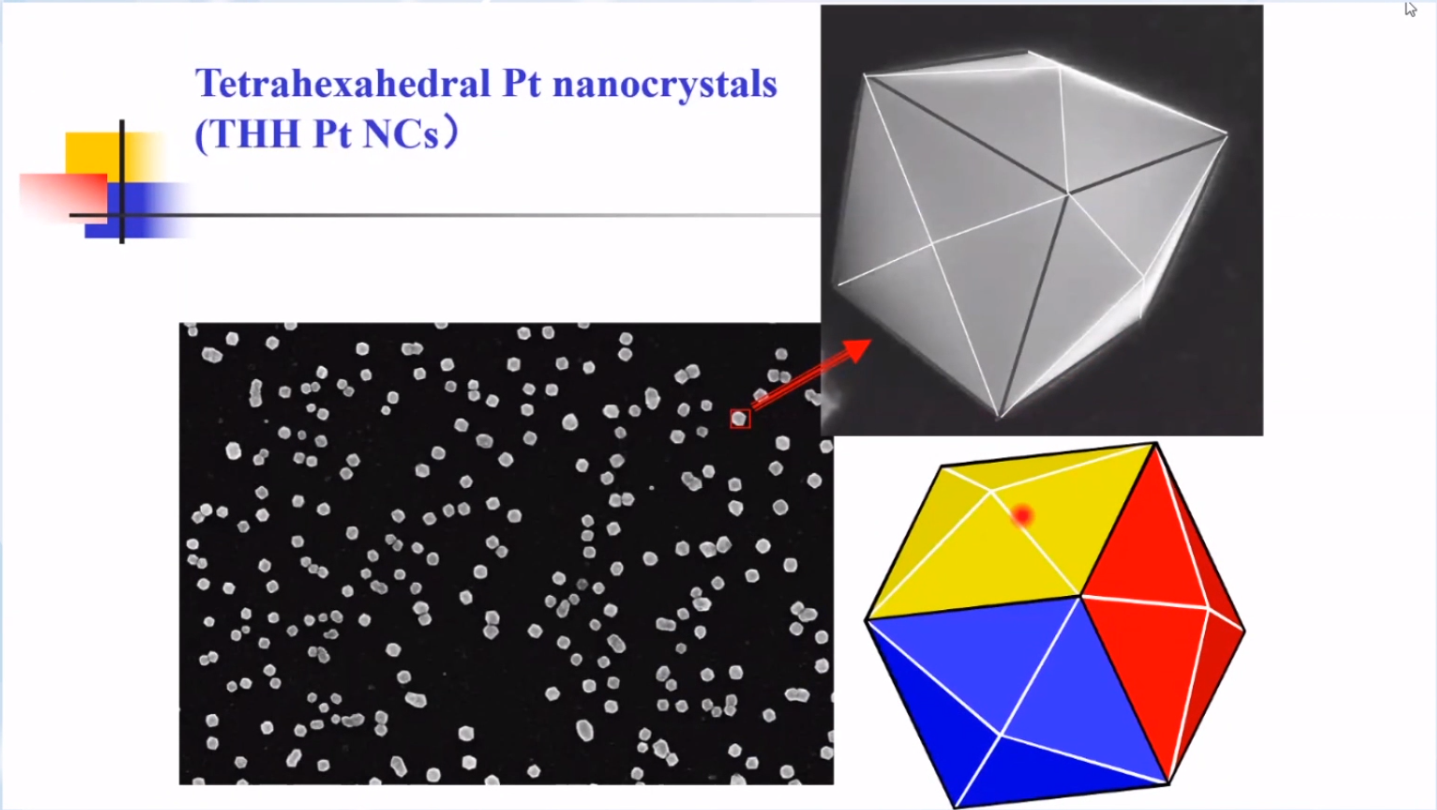
高指数晶面纳米催化剂的电化学制备:孙院士课题组于 2007 年首次实现了高指数晶面金属纳米催化剂的成功制备, 采用的是电化学方波电位法(反奥氏熟化过程), 得到高指数晶面结构的铂二十四面体(Pt THH)纳米晶催化剂 。
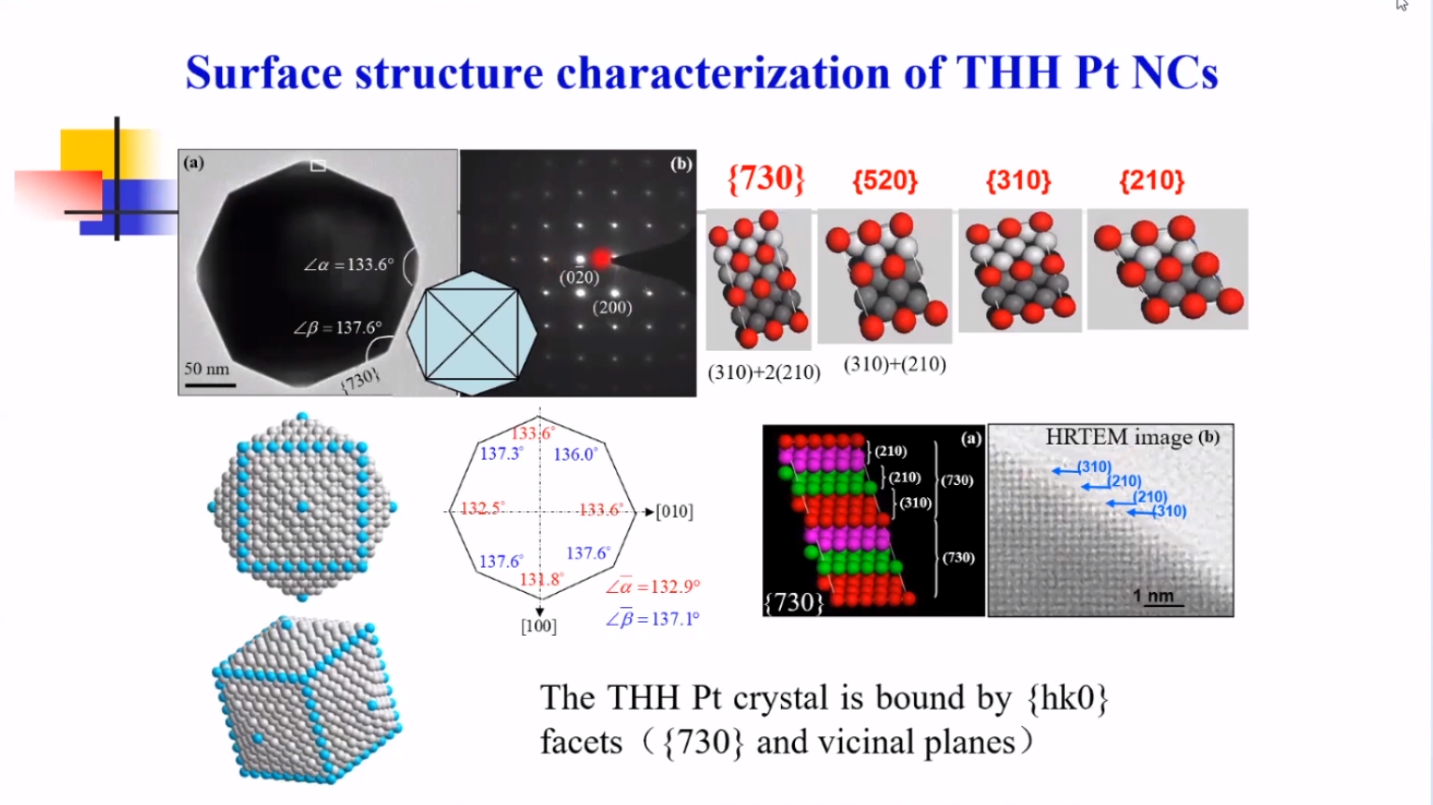
从 Pt THH 的高分辨透射电镜图可以看出,纳米晶表面为{730}高指数晶面,{730}由{210}和{310}晶面周期排列而成,这些高指数晶面含有较高密度的活性中心。
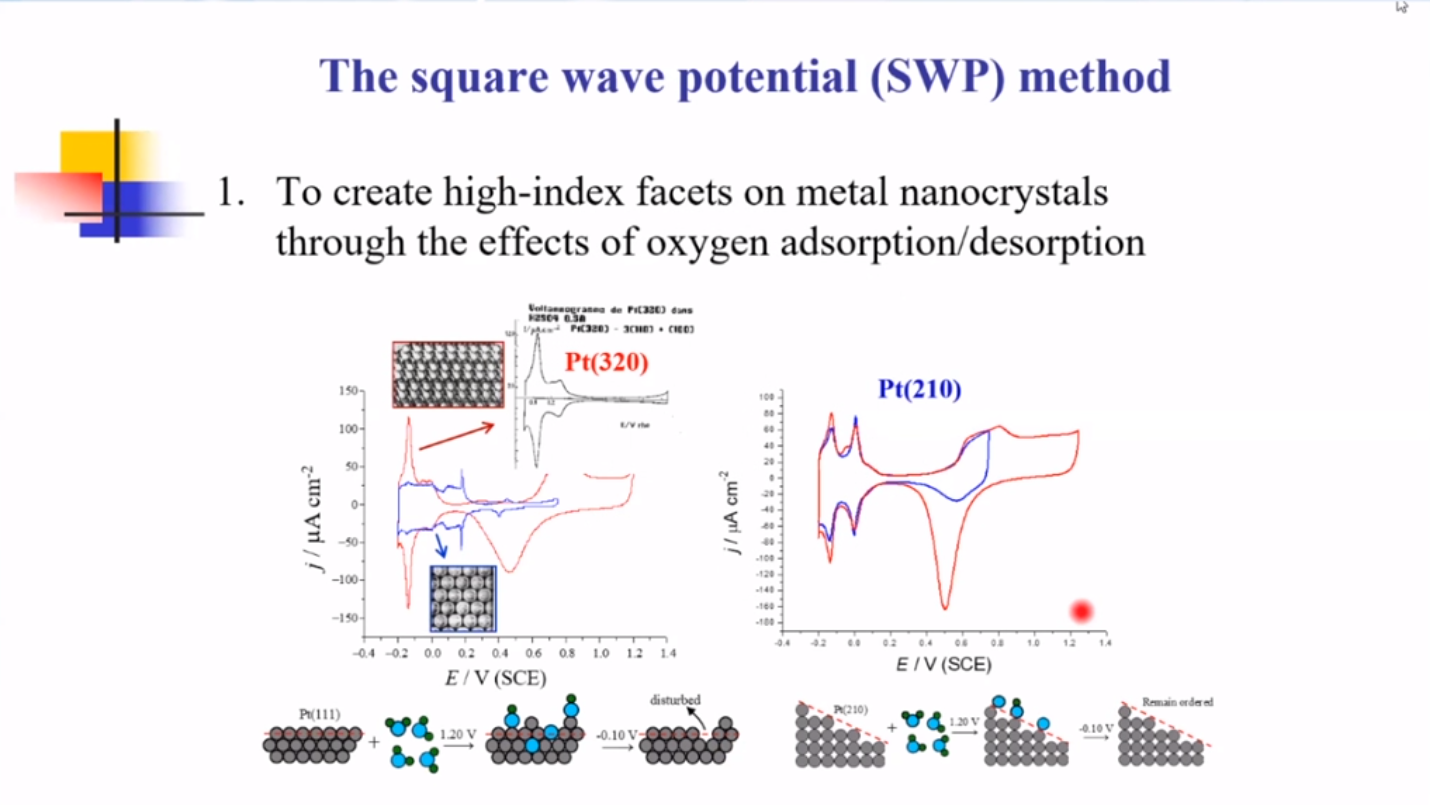

制备出高指数晶面结构的纳米晶的关键:
1、氧的吸附/脱附可以将金属纳米晶的平整表面变成台阶表面;
2、水分解物质的电化学吸附可降低高指数晶面的表面能;
3、施加周期性方波,高电位下通过氧的吸附选择高指数晶面结构,低电位下离子还原晶体生长。

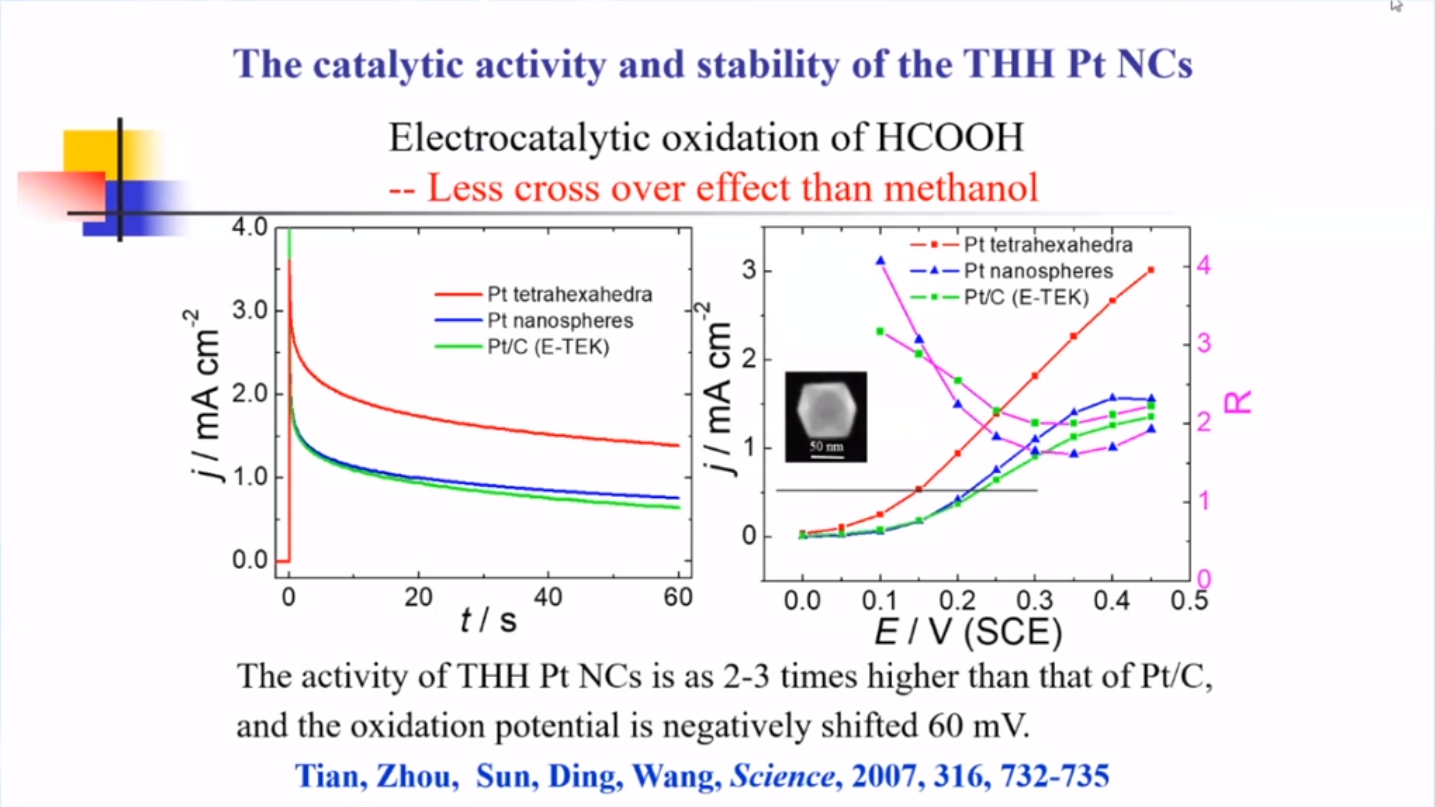
理论和实验结果证实,Pt THH 的催化活性更好,而且在稳定性以及起峰电位上都存在明显的优势。

Pt THH 还具有非常好的热稳定性,可耐受约 800 ℃的高温。
(三)纳米粒子模型催化剂
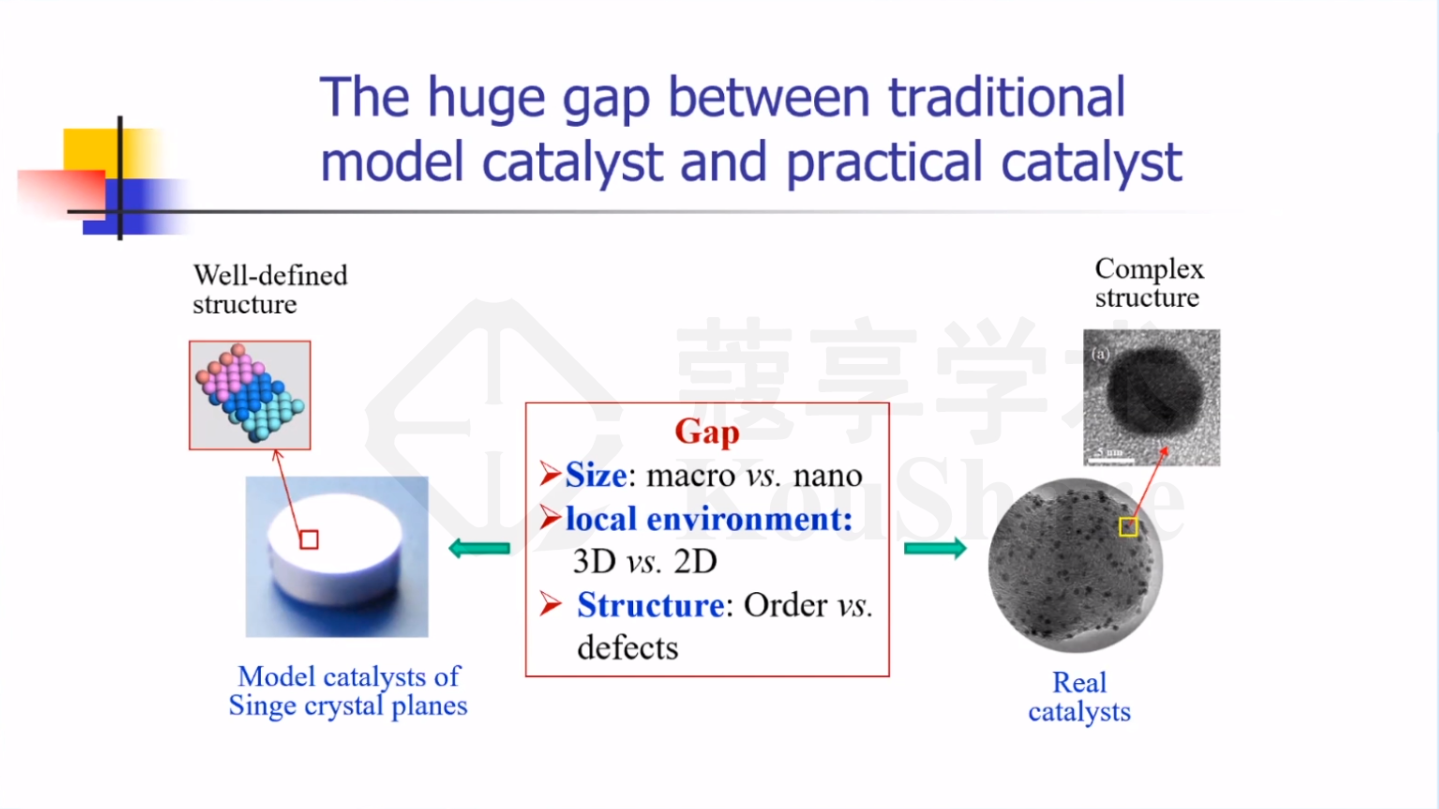
传统模型催化剂和实际催化剂在尺度、空间环境和结构方面存在巨大鸿沟。
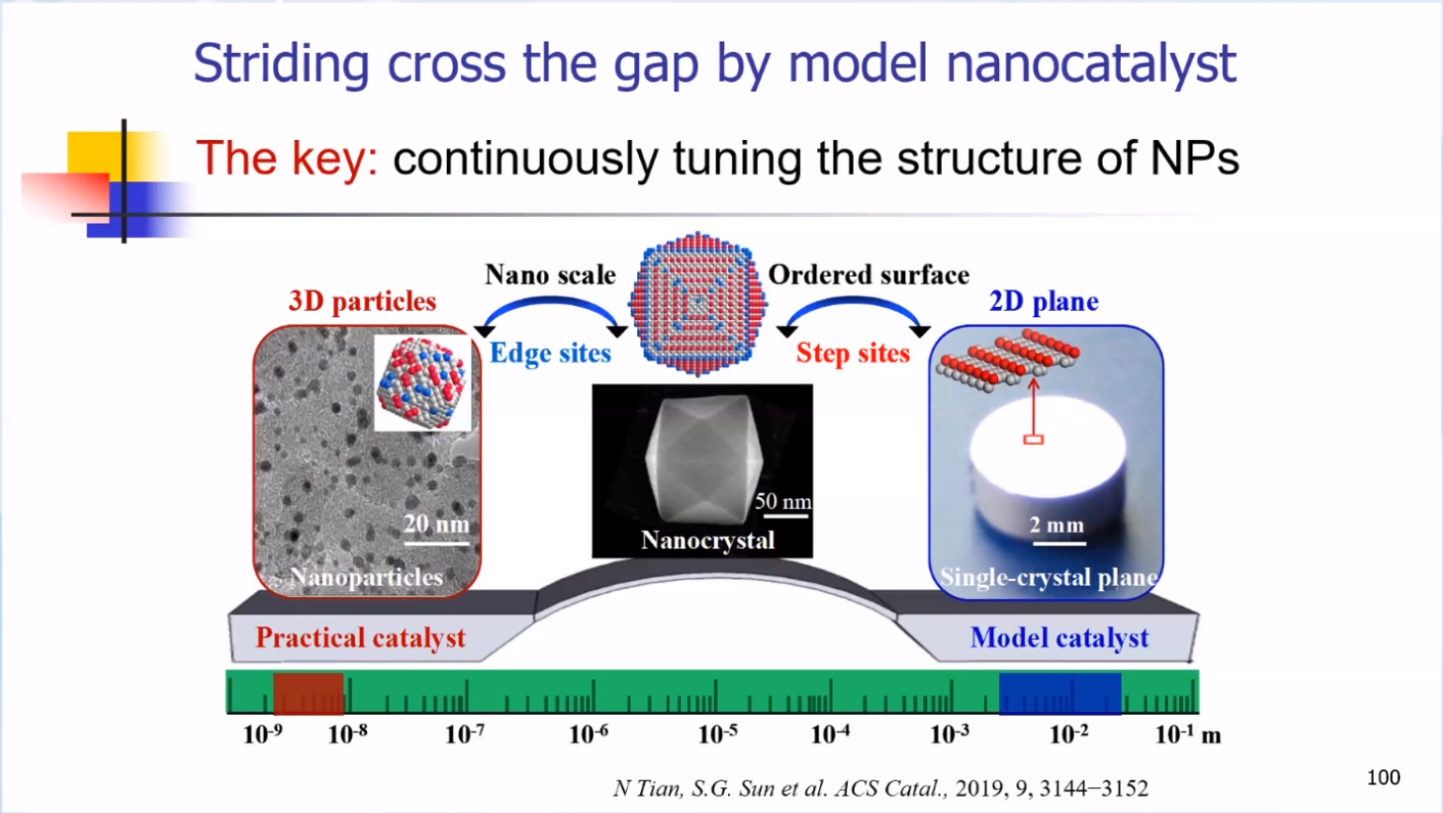
用表面结构明确的纳米晶作为桥梁来研究纳米尺度的模型催化剂的构效关系,从而进一步指导实际催化剂的设计和制备,关键点在于能够连续调变纳米催化剂的表面结构。
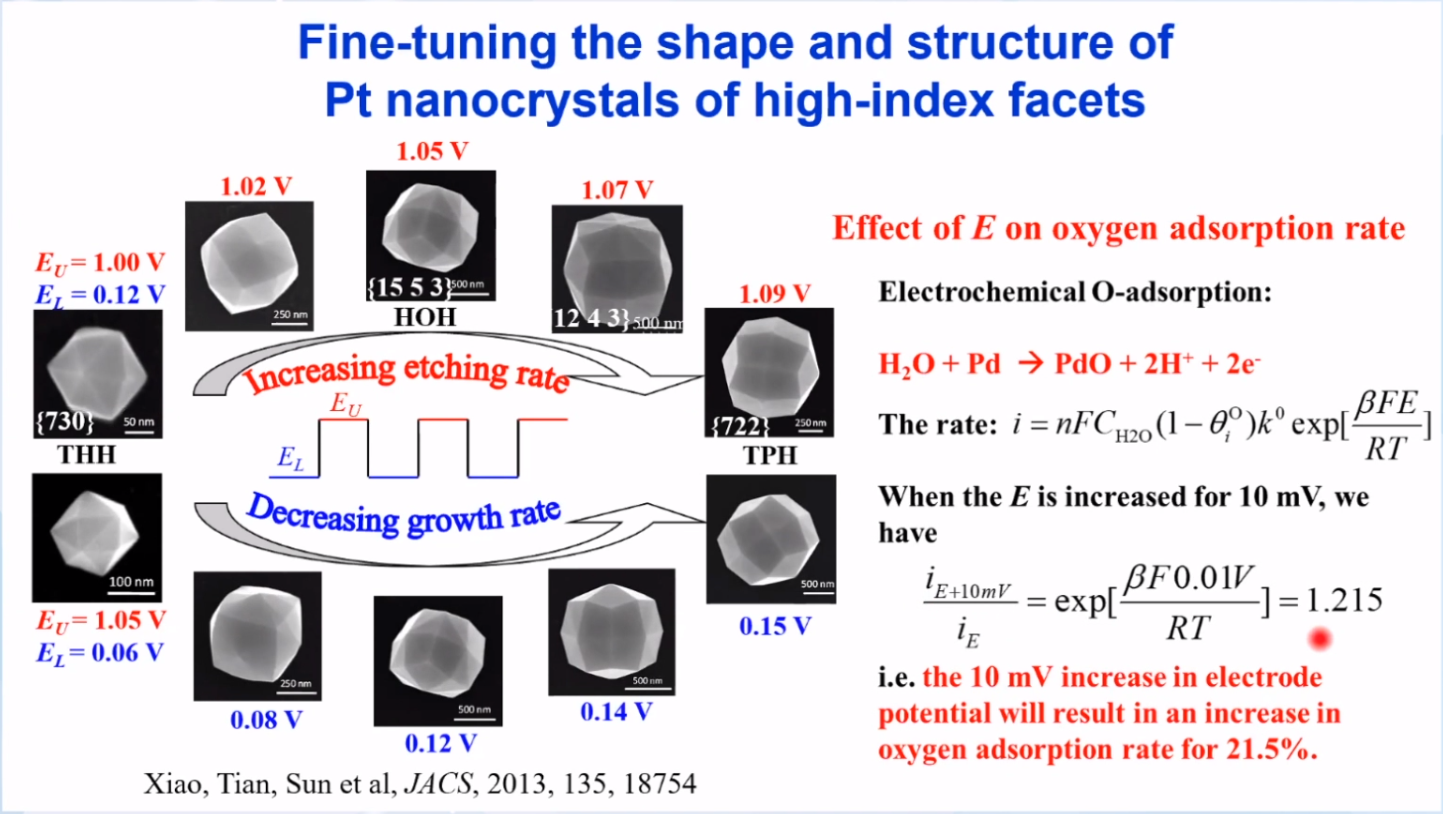
逐渐改变方波电位的上限或者下限电位, 可以连续调控 Pt 纳米晶的形貌。Pt 纳米晶的形状的变化,意味着其表面原子排列的类型同样发生了变化。如图所示,随着上限电位或下限电位的升高,Pt 纳米晶从THH转变为HOH,最后转变为TPH。总体来说,Pt 纳米晶的表面结构的连续调变是由上限电位的氧化刻蚀、下限电位的生长及由氧物质吸脱附引起的表面重构作用共同决定的。
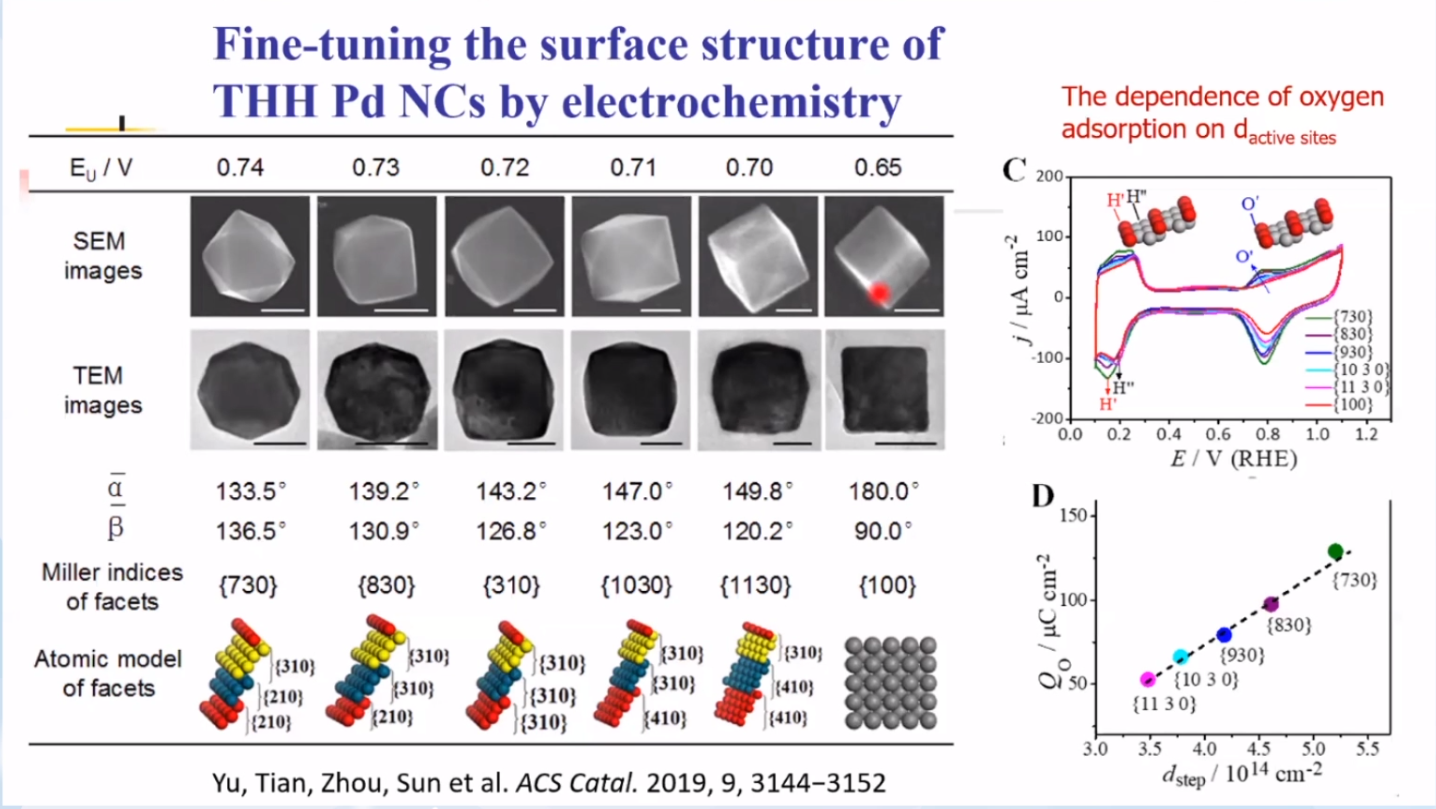
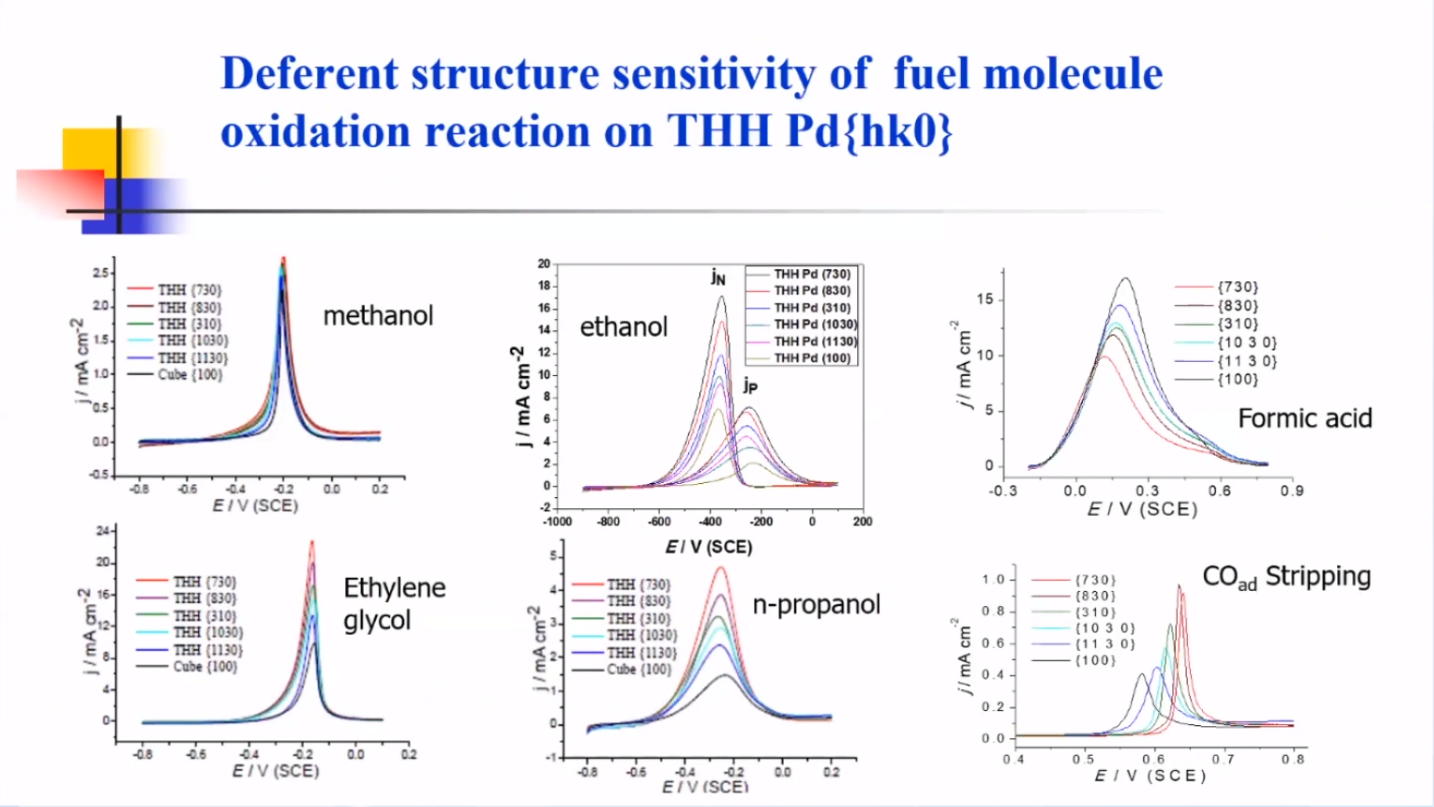
通过改变方波上限电位,孙院士课题组制备出一系列同样形状但表面结构连续发生变化的Pd NCs。
(1)对于甲醇来说,表面晶面指数改变对反应活性没有大幅度影响。
(2)对于乙醇、乙二醇、丙醇来说,表面晶面指数越高(即表面台阶位密度越大),反应活性越高。
(3)对于甲酸来说,表面晶面指数越高,反应活性反而下降。
纳米尺度上的构效规律与反应有关。同样的催化剂,对不同的反应,构效规律也是不一样的。
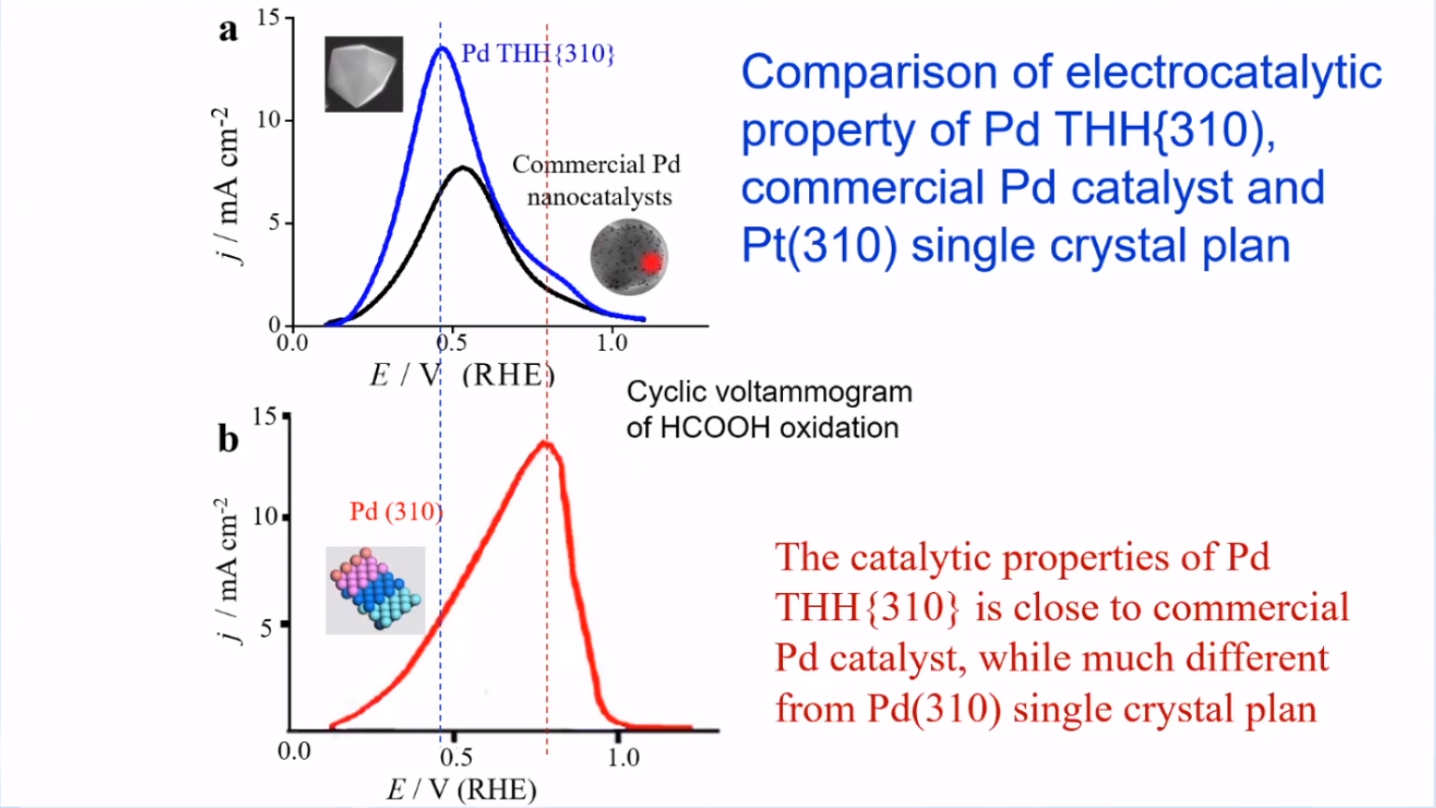
总体来说,高指数晶面的纳米晶体作为模型催化剂,其性能更接近实际催化剂。
(四)高指数晶面结构纳米催化剂

孙院士团队在高指数晶面纳米催化剂方面进行了持续深入的研究,主要包括:制备更小的粒径、表面结构设计、精细调控、不同金属的不同催化反应、不同电催化反应、量产技术发明和应用等。
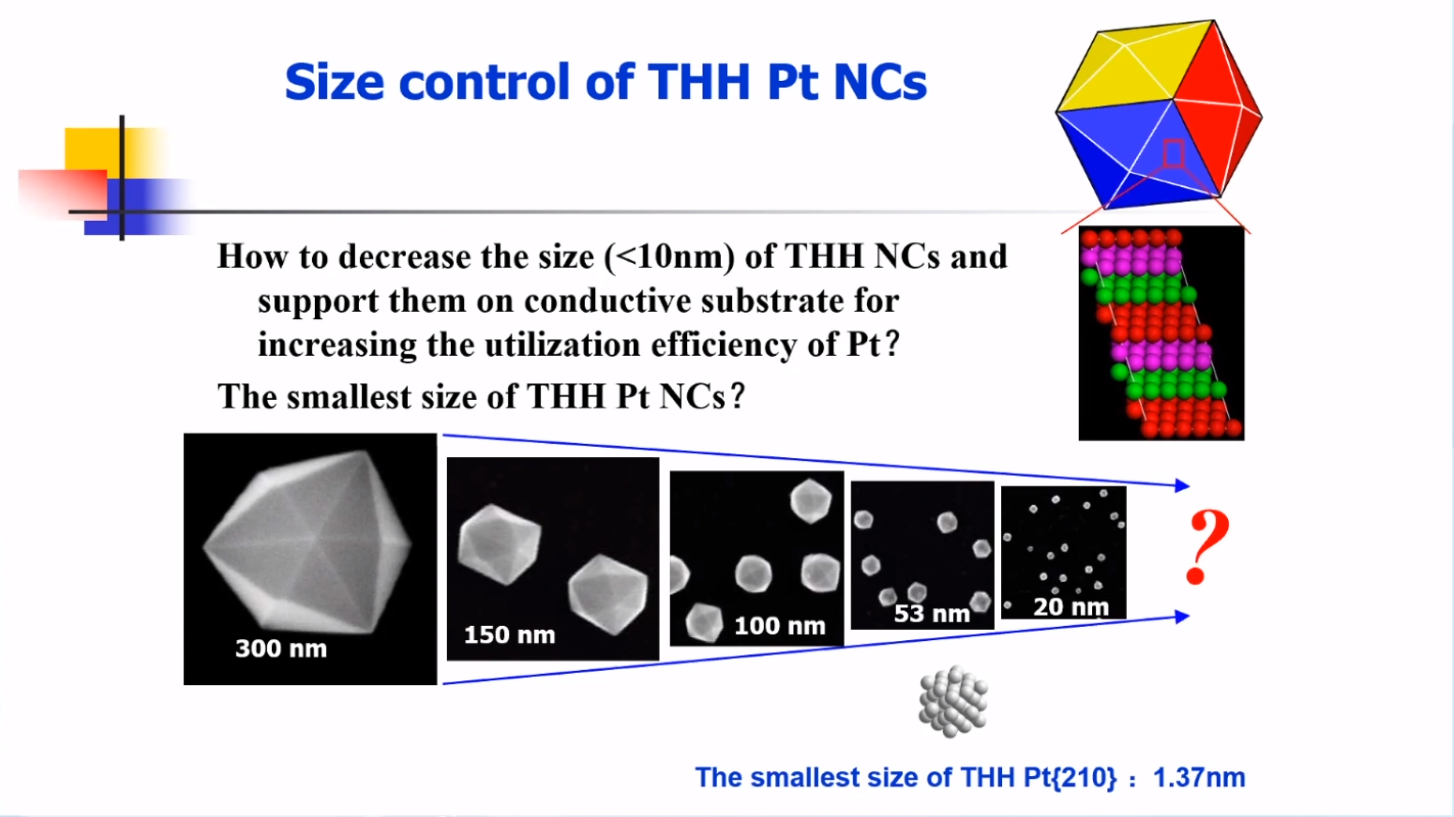
为了提高贵金属利用率、促进催化剂的实际应用,孙院士研究团队制备了小尺寸的高指数晶面纳米晶——小粒径铂二十四面体(Pt THH)。
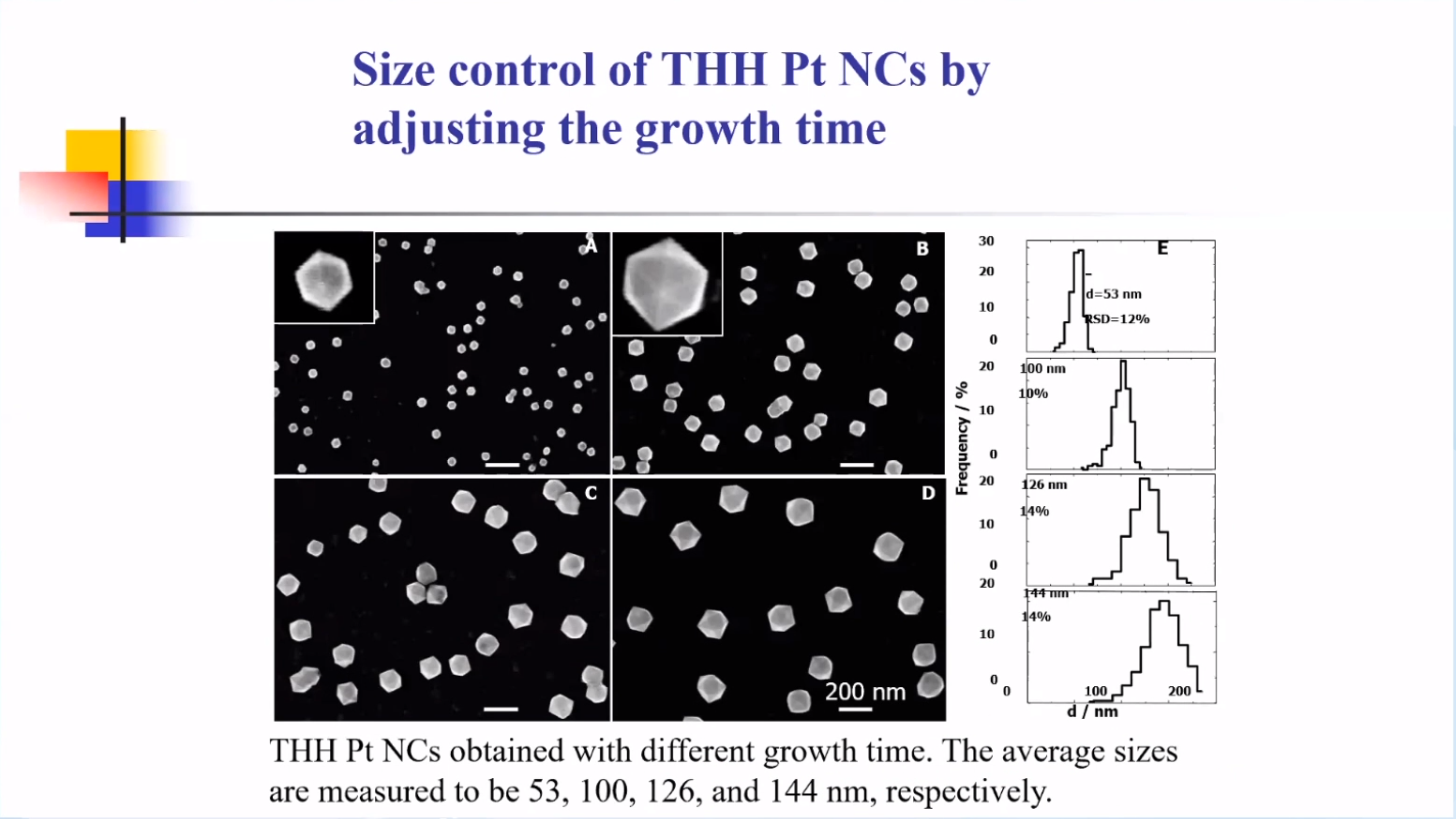
通过控制生长时间可以调控Pt THH的粒径大小。生长时间越久,粒径尺度越大。

通过方波处理可以将立方体纳米晶转变为二十四面体纳米晶。TEM和循环伏安测试结果说明纳米晶表面结构已经从(100)低指数晶面转变为高指数晶面。
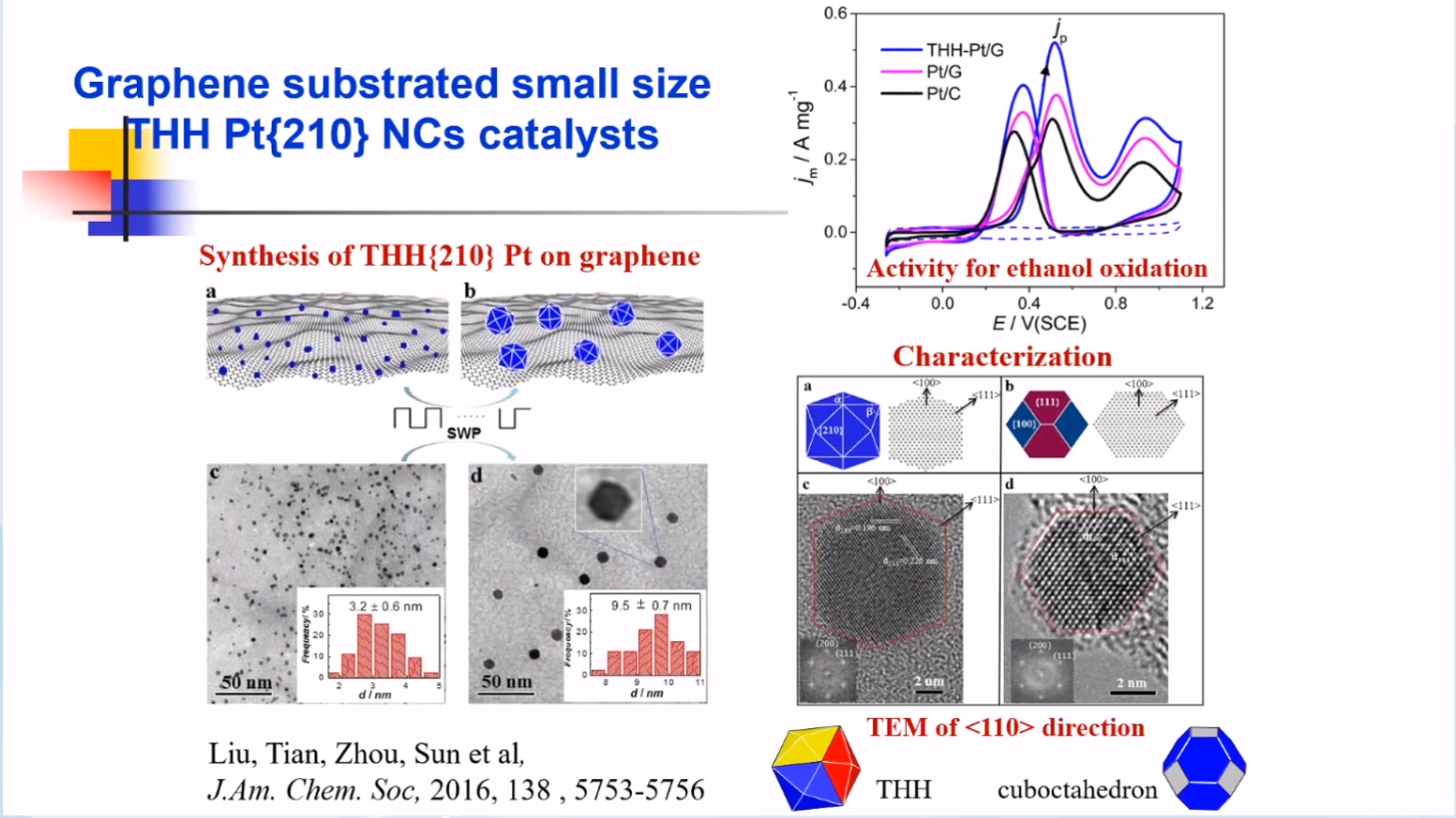
也可以直接在一些载体上制备得到高活性表面结构的纳米晶。如孙院士团队以石墨烯为载体,通过化学沉积、方波电位处理制备得到表面晶面为(210)的Pt THH 纳米晶。
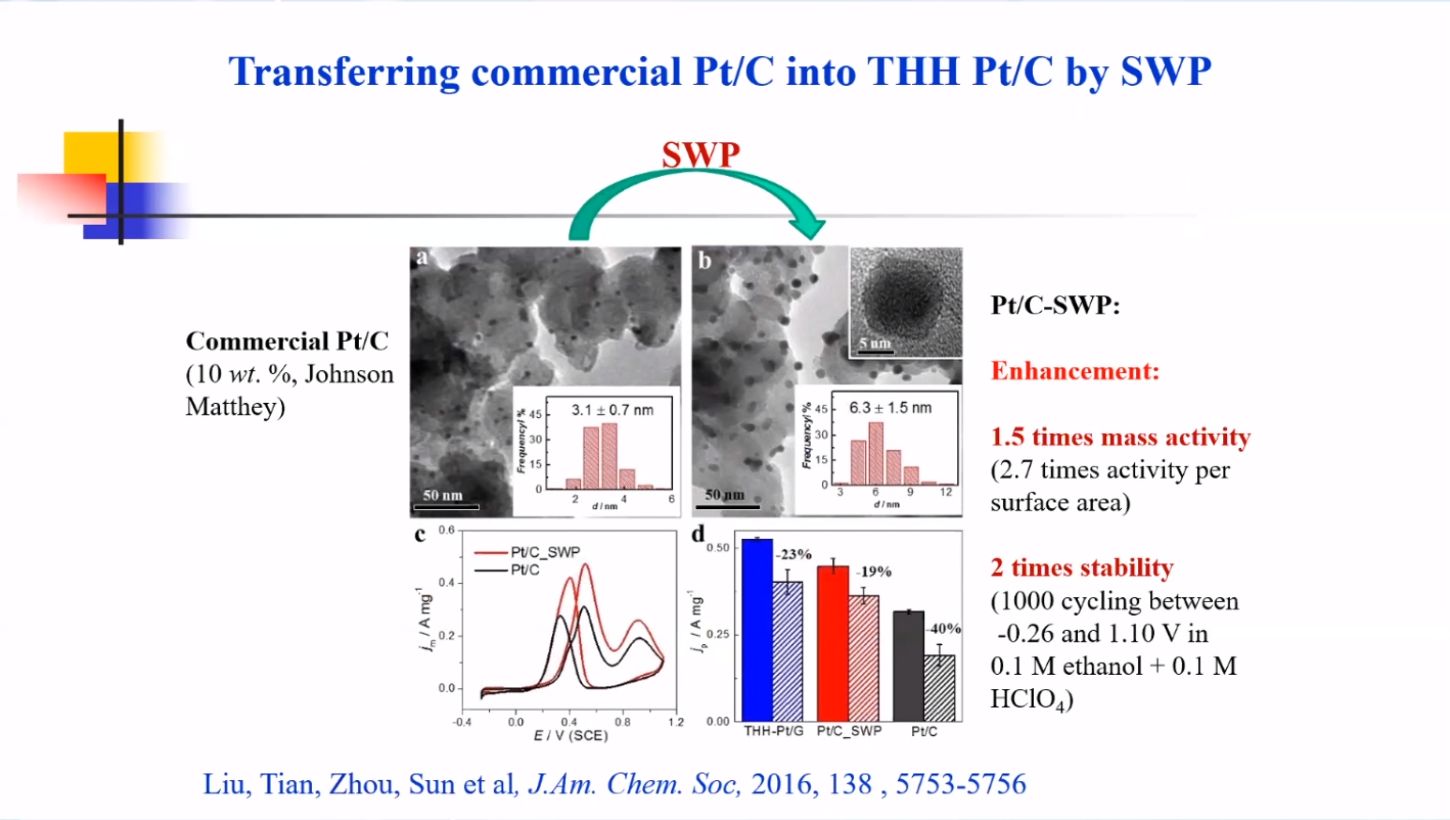
方波电位方法同样适用于处理商品催化剂Pt/C,使其表面重构,形成(320)等高指数晶面。电化学处理后 Pt 纳米粒子的粒径尺度从3.1 nm增加到 6.3 nm,稳定性提升了2倍。且由于面积比活性得到显著提高,使其对乙醇电催化氧化的质量活性提升了1.5倍。
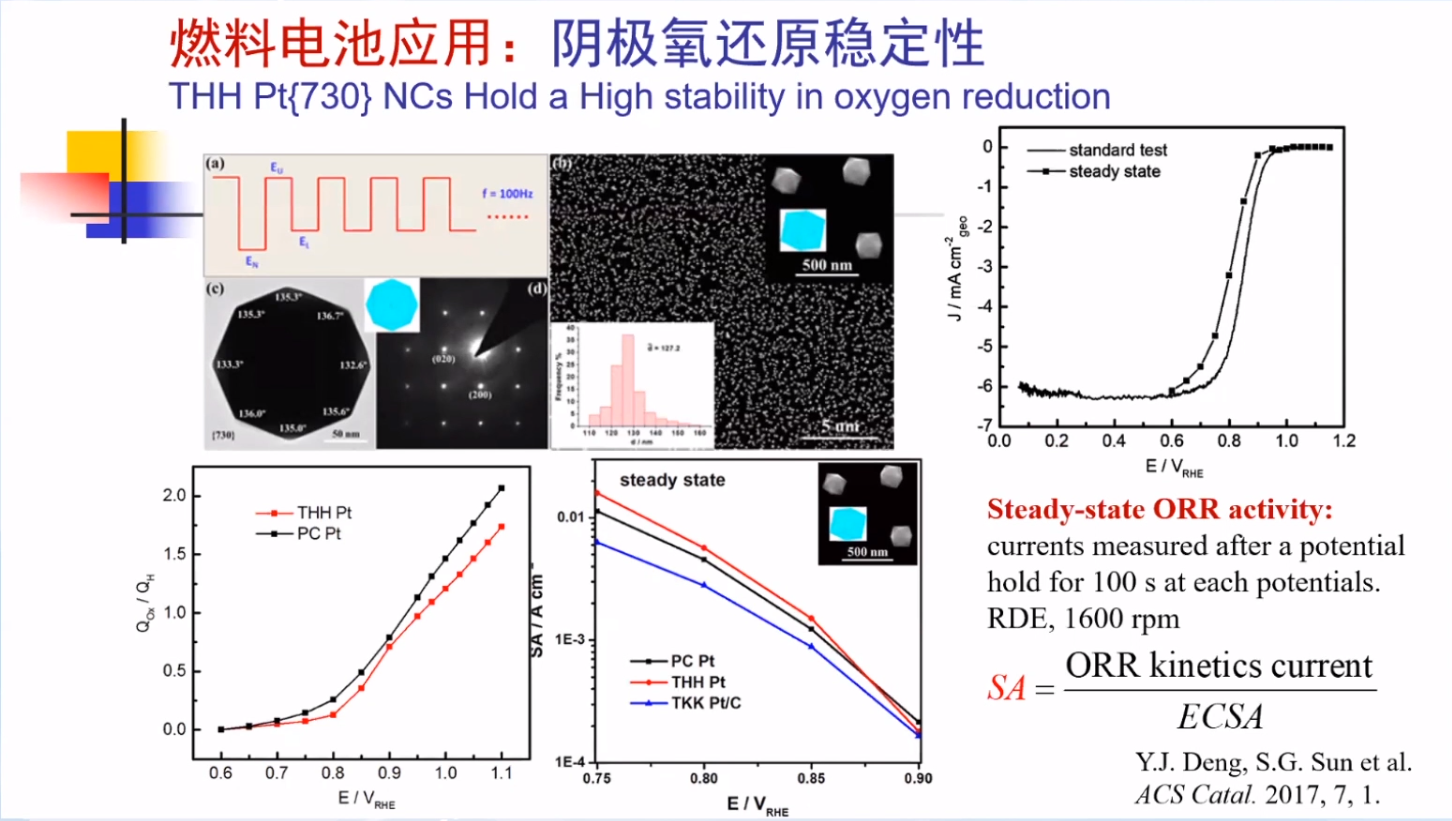
高指数晶面Pt纳米晶催化剂用于燃料电池的阴极氧还原反应仍表现出优异的稳定性。
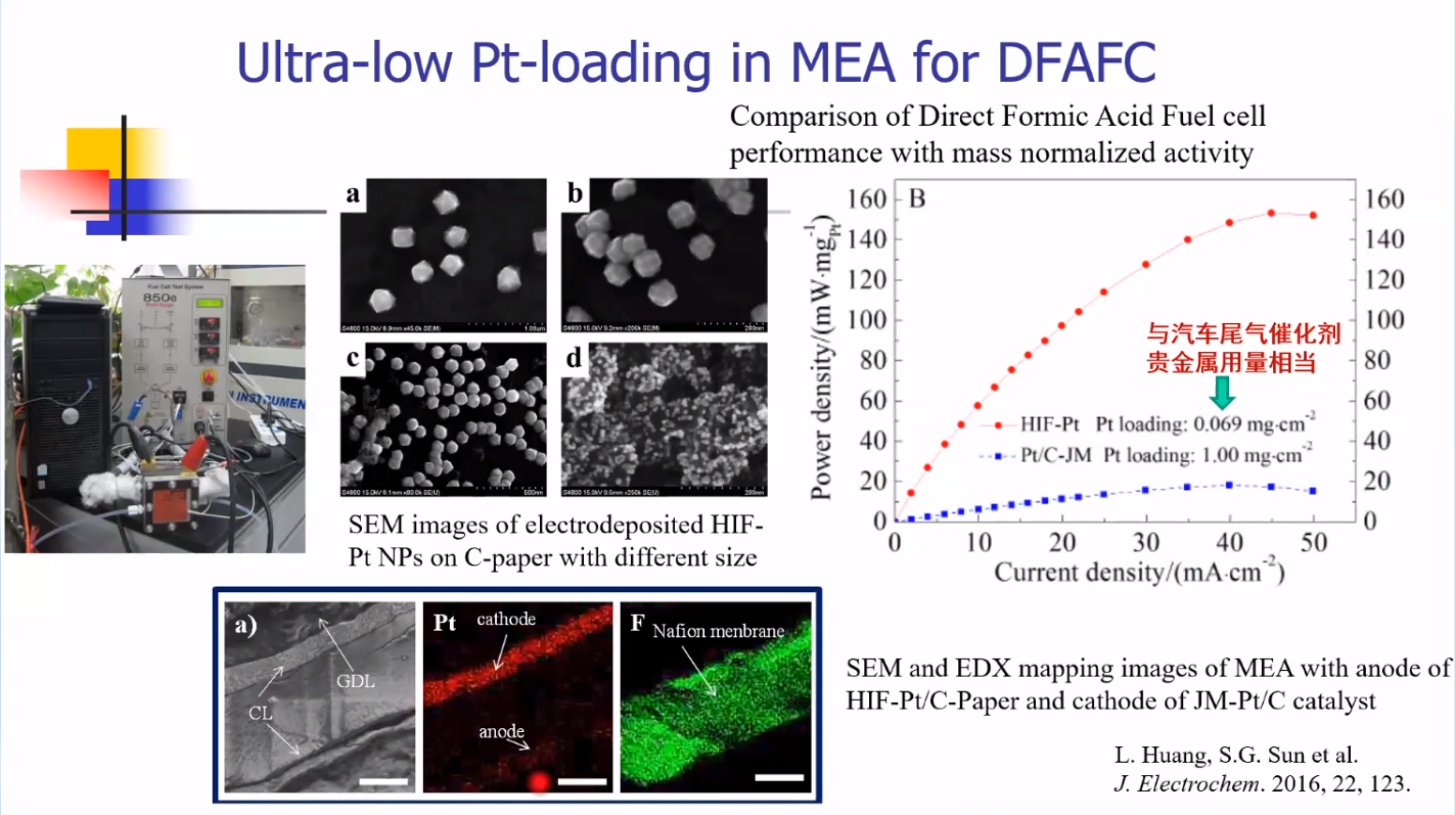
将高指数晶面的催化剂负载在碳纸表面,再热压到Nafion膜上制备得到了膜电极(MEA)。载量与汽车尾气催化剂贵金属用量相当,表明高指数晶面催化剂在未来的实际应用中具有很大的前景。
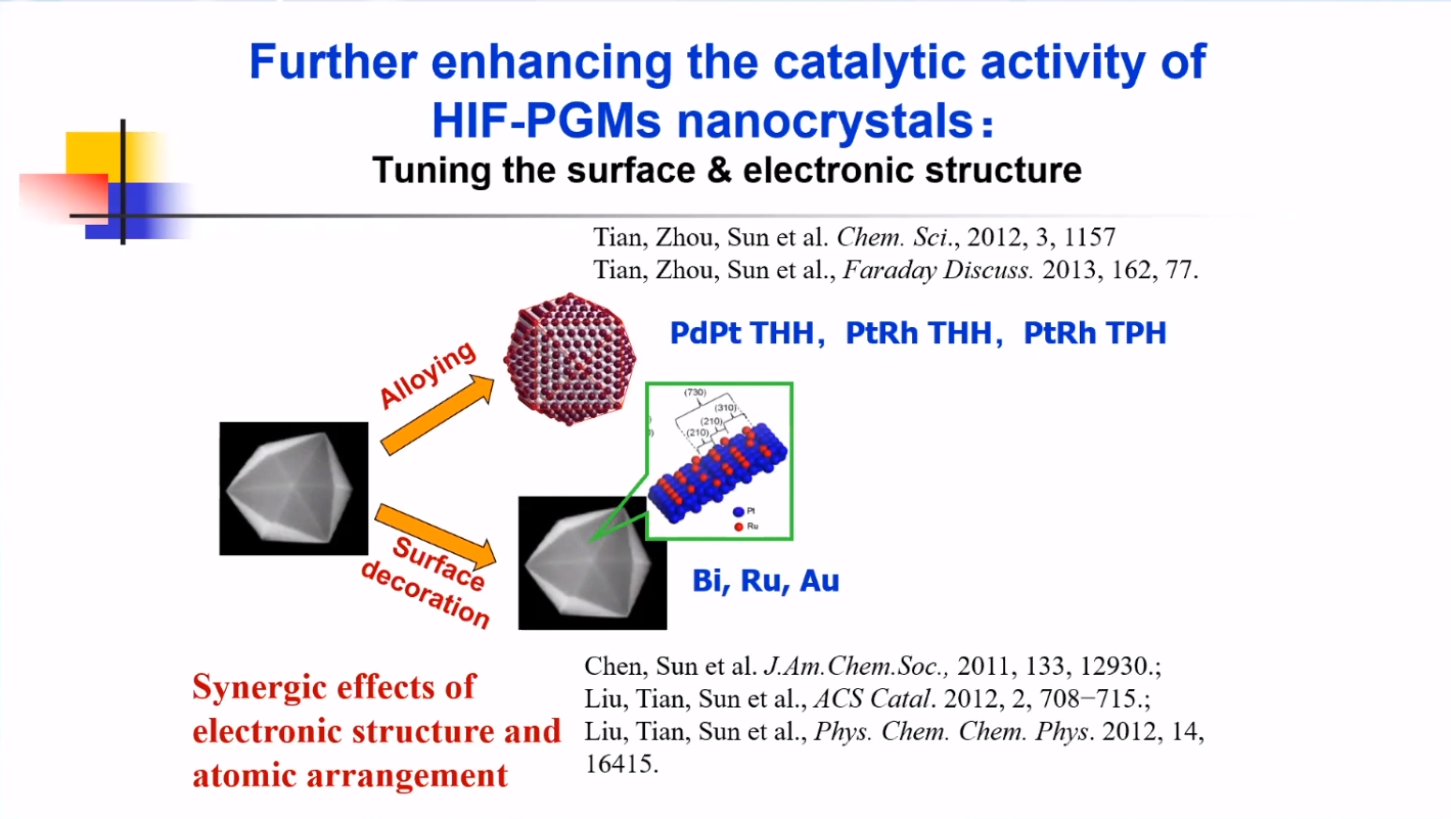
通过调控表面和电子结构可以进一步提升催化剂性能。
调控表面和电子结构有两种方式:一是制备出合金高指数晶面纳米粒子,如PdPt THH纳米晶以及PtRh THH/TPH纳米晶;二是表面修饰单原子层/多原子层,如Bi, Ru, Au。
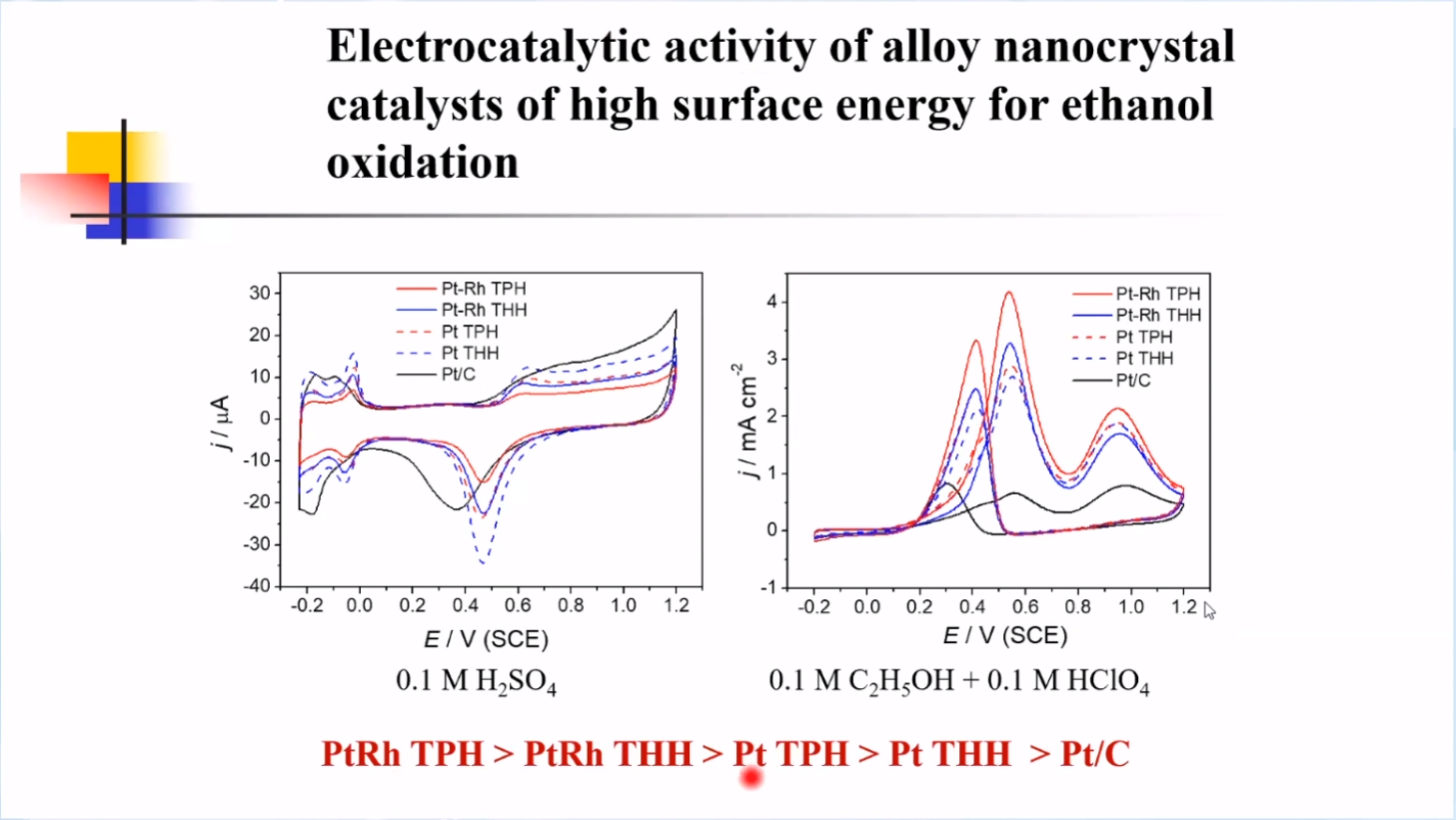
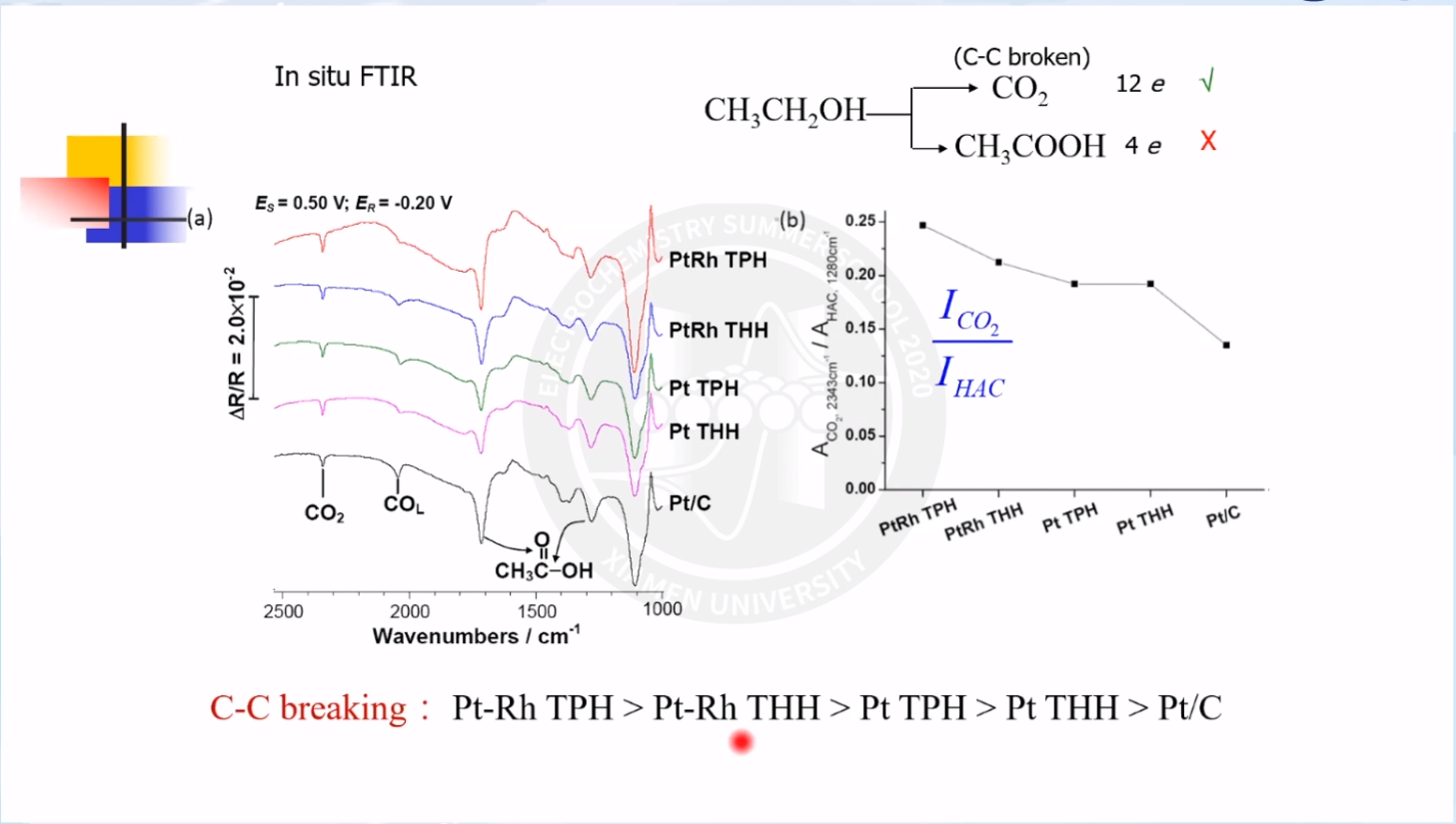
孙院士课题组制备了一系列合金高指数纳米晶,均在保持表面结构同时改变电子结构。实验结果表明,合金纳米晶催化剂对有机小分子的电氧化表现出更优异的催化性能,其中催化活性比较如下:PtRh TPH>PtRh THH>Pt TPH>Pt THH>Pt/C。
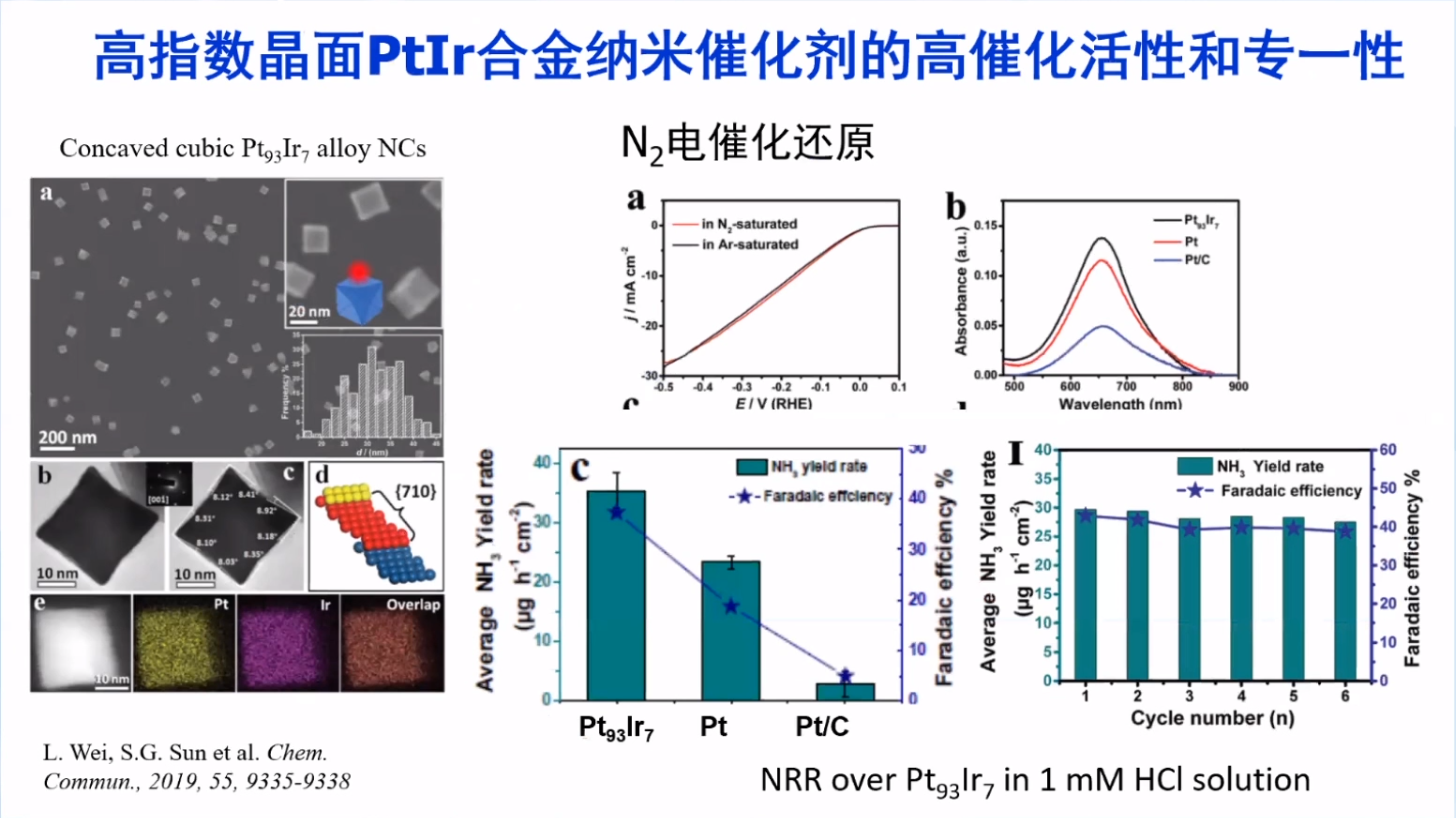
高指数晶面PtIr合金纳米催化剂可以将N2还原为NH3,产率远优于商品催化剂Pt/C。
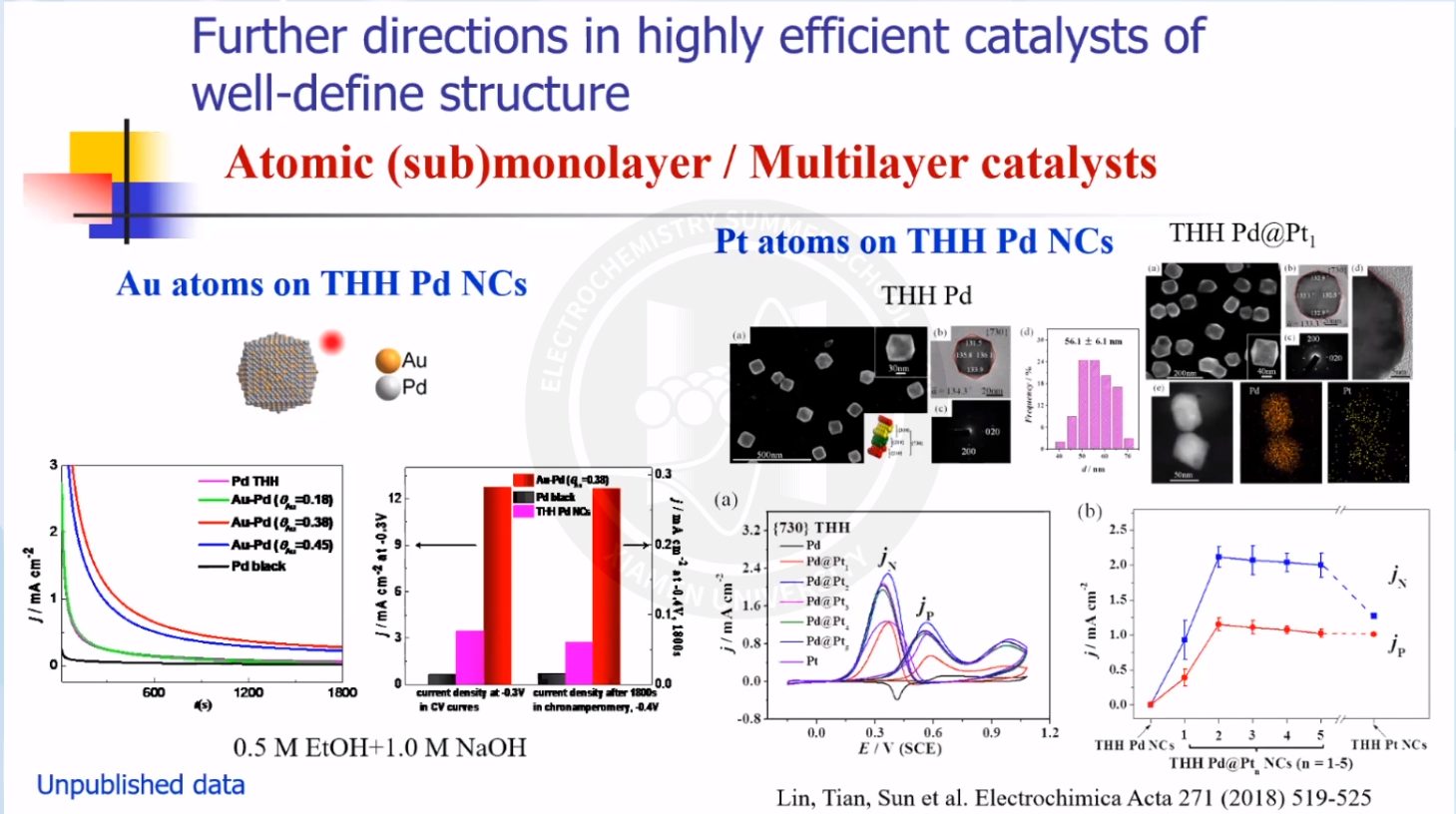
孙院士课题组通过在Pd THH 纳米晶表面修饰其它金属原子,明显提高了其催化性能。如在Pd THH表面修饰Au/Pt单原子层/多原子层。
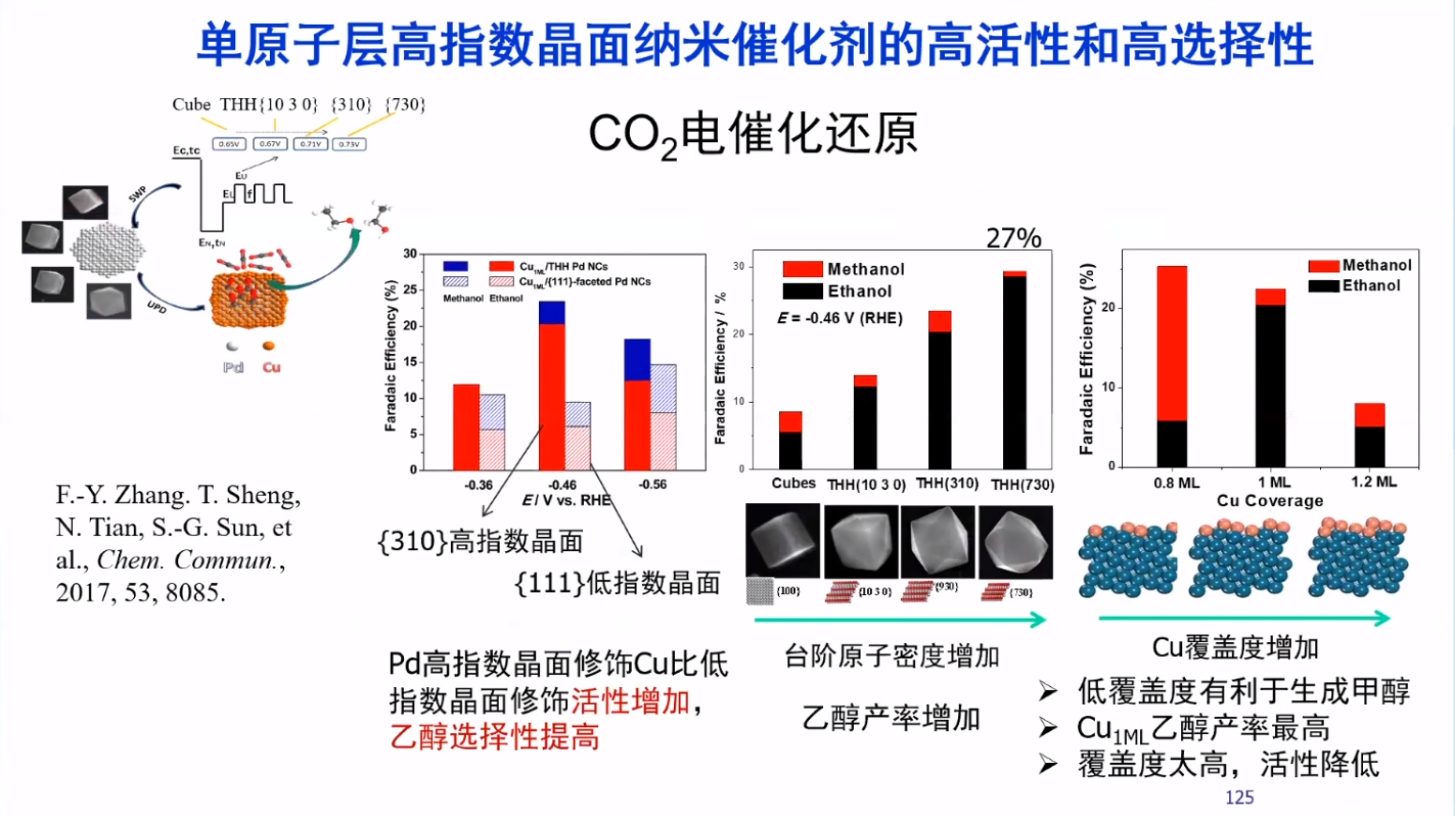
为了解决环境污染、把CO2还原成高附加值的液体燃料/化学产品,孙院士课题组采用表面修饰的方法,在Pd THH表面修饰Cu原子以提高其对CO2还原的电催化性能。研究表明,在高指数晶面Pd上修饰Cu,生成乙醇选择性更高。同时,在Pd THH 表面修饰单层Cu时,乙醇产量最高。即对于此类催化剂,亚单层或单层即能实现高效的CO2定向转化,Cu覆盖度太高,活性反而降低。
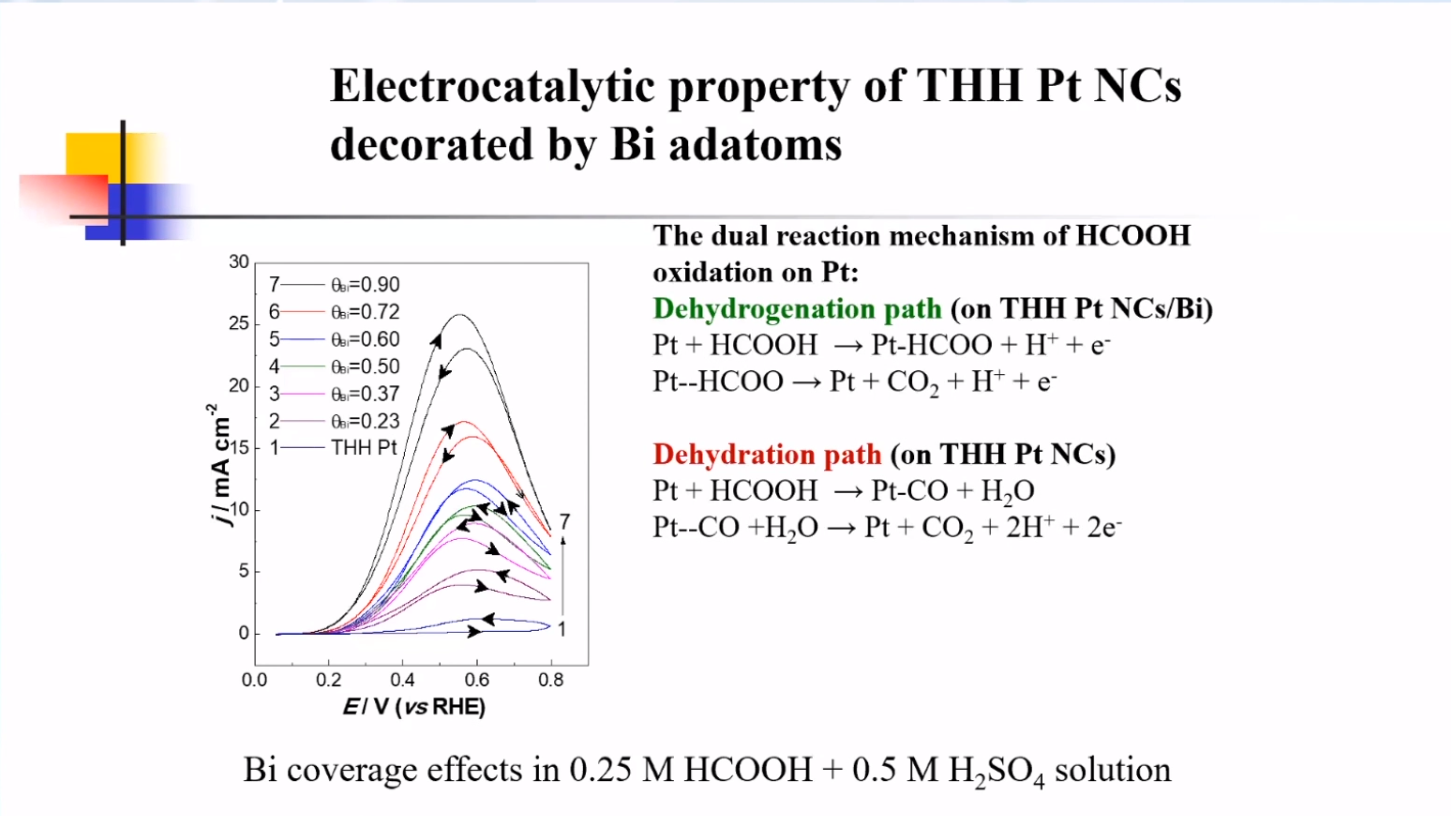
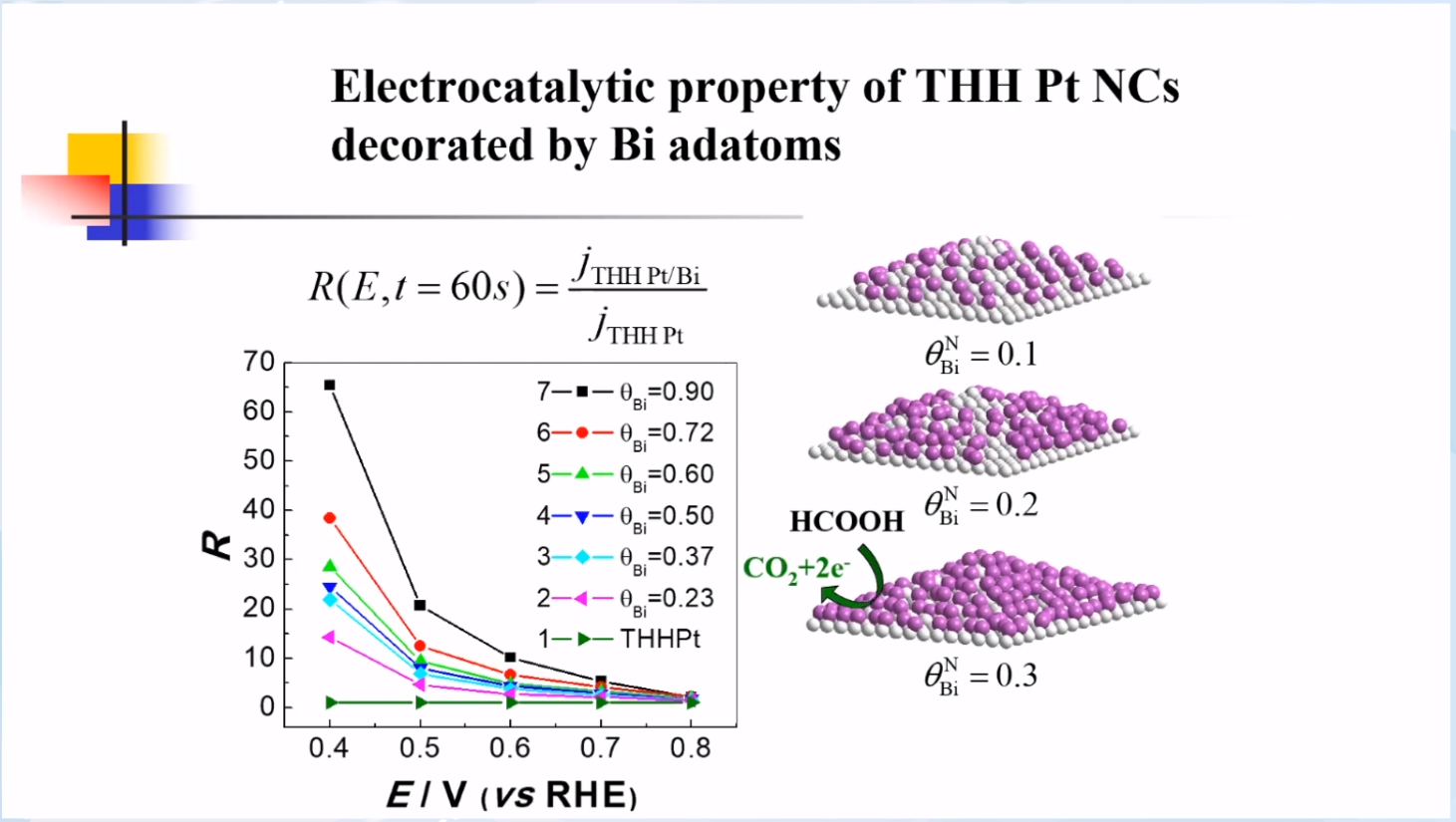
在Pt THH 表面修饰 Bi 原子,凭借第三体效应(阻止了甲酸的碱性吸附)和电子结构效应的协同作用,其对甲酸的催化活性有了大幅度的提高。

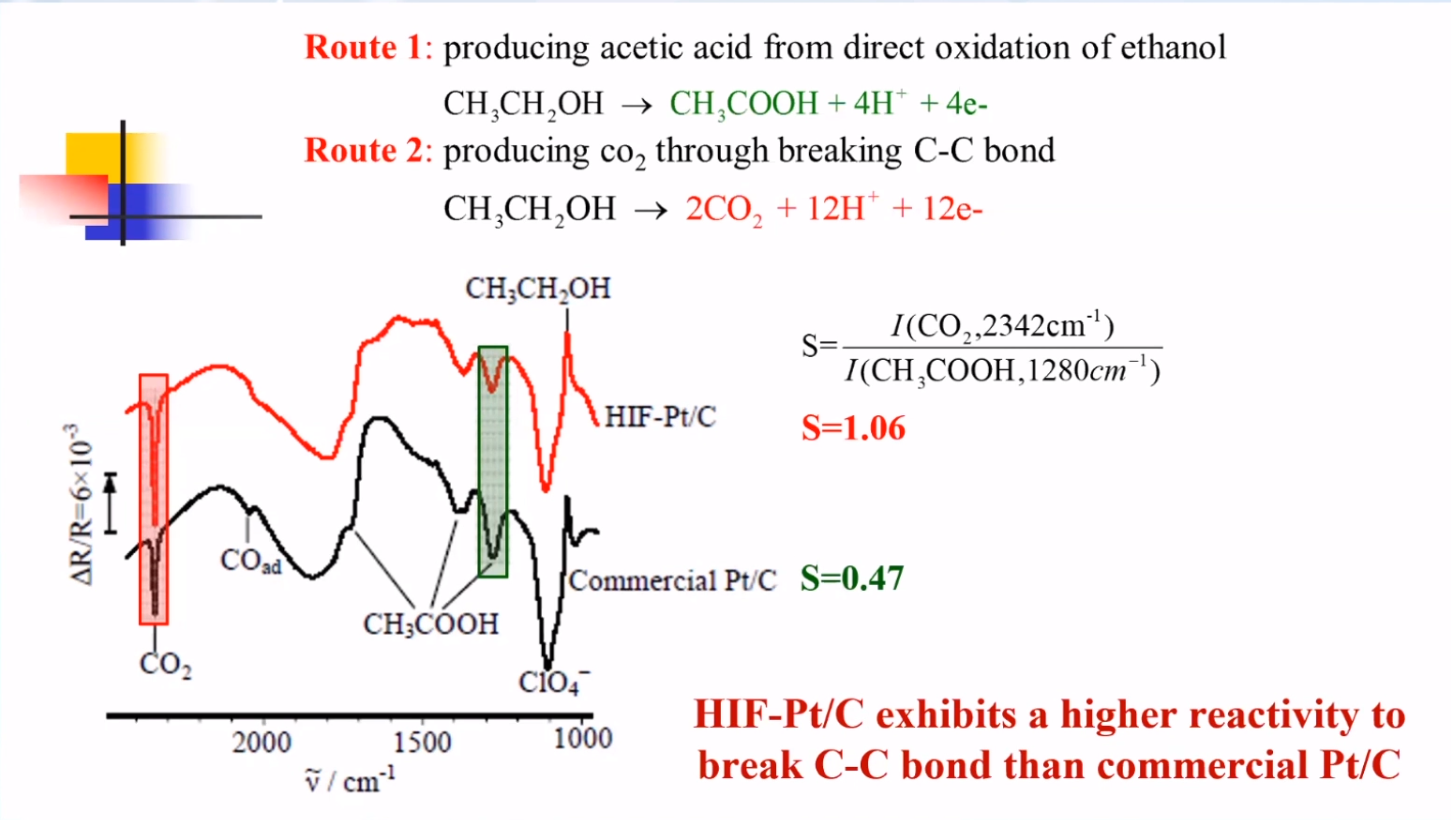
通过分子水平分析发现,断裂乙醇中C–C键的活性,是提升DEFC(直接乙醇燃料电池)法拉第效率的关键。以HIF-Pt/C高指数晶面结构催化剂和Pt/C商品催化剂为例,探究高指数晶面结构催化剂的作用机制。通过红外光谱测试跟踪反应过程发现,确定两种催化剂均涉及两种反应途径,但断裂C–C键的效率不同,HIF-Pt/C断裂C–C键的效率是Pt/C的二倍以上。
四、结论

