
Recent advances in platelet engineering for anti-cancer therapies (Open Access)
吕岩霖,魏炜,马光辉*
Keywords: Engineering platelets; Platelet-mimicking; Drug delivery; Anti-cancer therapy
DOI: 10.1016/j.partic.2021.09.006
血小板能在血管损伤部位进行聚集,促进血液的凝固,在止血过程中起到重要作用。鉴于血小板的这一功能,以及血小板与免疫反应的密切关系和与癌细胞之间的相互作用,人们开发了许多基于血小板(或血小板膜)的仿生工程策略,用于抗肿瘤治疗。
近日,中国科学院过程工程研究所生化工程国家重点实验室的马光辉院士、魏炜研究员和吕岩霖副研究员在PARTICUOLOGY上发表综述,概述了该领域最新的几项创新工作,提出利用血小板(或血小板膜)规避机体的免疫清除反应,能将各类抗肿瘤药物制剂高度特异性地递送至肿瘤部位甚至肿瘤深处,可实现肿瘤的有效清除、抑制肿瘤的复发和转移。最后展望了基于血小板的仿生抗肿瘤治疗的未来方向。
欢迎感兴趣的读者扫描下方二维码进入Science Direct官网免费阅读、下载!

文章简介
药物对肿瘤的靶向和在瘤内的渗透是抗肿瘤治疗中长期存在的重要问题。为了提高药物在肿瘤部位的聚集,人们利用纳米级载体在肿瘤血管的EPR效应实现药物对肿瘤的被动靶向。近年来,仿生颗粒因其独特的优势而日益受到关注。颗粒的生物源性使其具有优异的生物相容性,减轻免疫原性,并能实现对肿瘤的主动靶向。在这些仿生颗粒中,利用血小板进行抗肿瘤治疗的策略正在被广泛研究。由巨核细胞产生的血小板是一种天然的、多功能的药物载体,它们体积相对较小,没有细胞核,在减轻血管损伤和通过聚集在损伤部位凝血来止血等方面起着密切的作用。血小板还能识别血液中的循环肿瘤细胞并与之相互作用,并可以通过结合肿瘤细胞表面的特异性同源信号分子,选择性地靶向肿瘤。血小板的这些生理特性使其能够作为工程化肿瘤特异性药物递送和增强肿瘤内渗透的高效载体。文章概述了基于血小板的工程化抗肿瘤治疗的一些开创性工作,比较了使用单一或混合血小板膜、全血小板装载纳米颗粒的相对优势,讨论了利用工程化血小板产生载药的血小板衍生微粒在肿瘤部位的渗透。由于血小板的生物源性和装载药物的灵活性,这一仿生策略的有效性已经从动物研究中得到证实,有望进一步推进临床试验。
图文精读
基于血小板工程化的仿生策略可大致分为两种,一种是内在策略(阴),一种是外在策略(阳)。对于内在策略,血小板通过装载具有多种性质的各种抗体或颗粒而被赋予更多的性能;对于外源策略,提取血小板膜以覆盖不同的颗粒,以增强伪装和靶向能力,通过血小板膜与其他生物膜的杂合,可以获得更多特性。通过整合“阴”和“阳”,构建了多功能血小板仿生颗粒递送体系,以解决抗肿瘤治疗中的肿瘤靶向性和肿瘤内渗透问题。
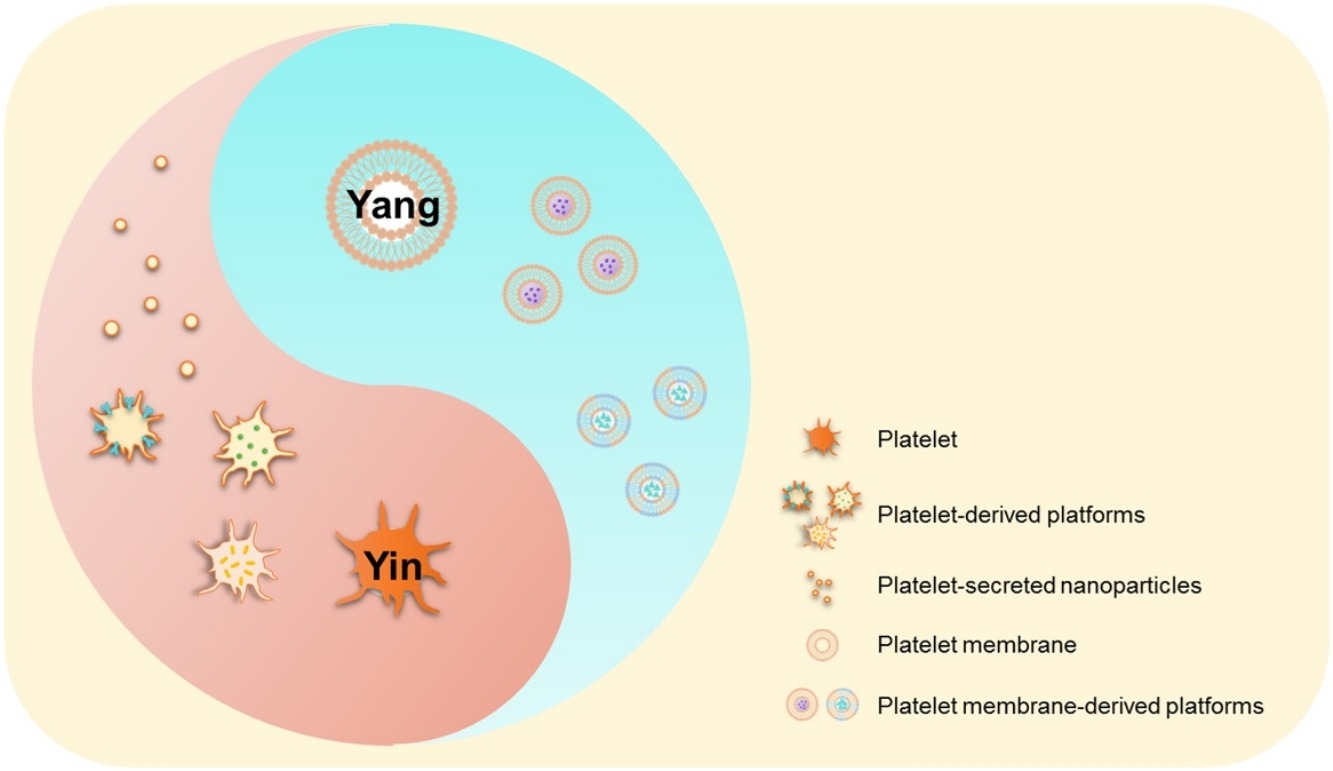
图1. 基于血小板工程化的仿生策略
与使用单一或混合血小板膜构建的靶向给药系统相比,使用全血小板作为靶向肿瘤和深度渗透的载体可以为抗肿瘤治疗提供更简单、更方便的途径。以其中一项工作为例:
血小板天然粘附受损血管并能在激活状态下形成血栓和分泌纳米囊泡,受此启发,将具有高光热转换效率的聚合物纳米颗粒和免疫激动剂温和高效地导入血小板中,在体内借助血小板的天然性质,选择性地粘附于有缺陷的肿瘤血管部位。在低功率近红外光照射下,光热所引起的肿瘤局部急性血管损伤可激活粘附的血小板,通过级联效应在肿瘤血管处形成血栓,以此形成光热纳米颗粒和免疫激动剂的“弹药库”。富集的血小板在上述激活状态下还可进一步分泌纳米级血小板囊泡,将光热纳米颗粒和免疫激动剂运送到肿瘤组织深处。这样不仅有利于光热清除更多的肿瘤细胞,还可以增强肿瘤抗原的免疫原性,完全抑制肿瘤的转移和复发。
所装载的纳米颗粒、药物等具有很好的灵活性,并且血小板可从患者或者供体获得,因此,该血小板仿生剂型在肿瘤个体化精准治疗领域具有较好的临床应用前景。
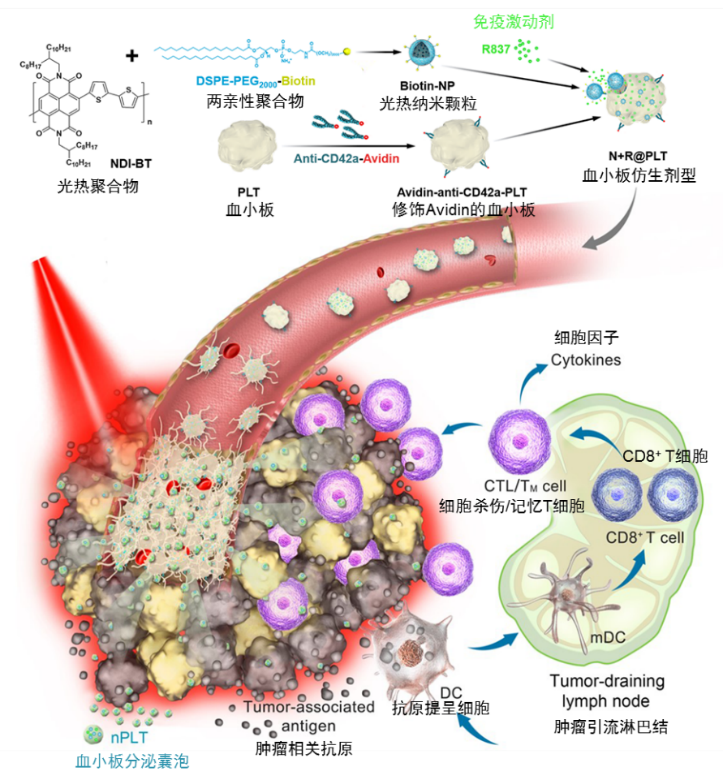
图2. 基于血小板的仿生剂型在抗肿瘤联合治疗中的作用
总结与展望
血小板是一种小而无核的细胞结构,具有多种多样的功能。通过利用其天然的生理学特征,基于血小板和血小板膜的药物递送策略显示出良好的前景,尤其是在抗肿瘤治疗中表现出优异的治疗效果。尽管以血小板为基础的仿生制剂在抗癌治疗方面具有巨大潜力,但仍有一些挑战阻碍了其临床应用。首先,血小板和肿瘤细胞之间相互作用的具体机制尚未解决,这可能增加治疗期间可能出现副作用的风险。其次,这些仿生策略在规模化和工业制造方面仍有多重独特挑战。最后,确保最终产品的纯度和长期储存所需的特殊要求对其商业化也提出了额外的挑战。目前和未来将致力于探索体内血小板衍生仿生制剂的药代动力学、安全性和分子/生理相互作用,以提高其临床转化的可能性。
作者介绍

马光辉院士1993年获日本东京工业大学博士学位,曾获国家“杰出青年科学基金”(2001)等人才项目,目前任中国科学院过程工程研究所生化工程国家重点实验室主任,Particuology生物颗粒主题编辑。主要从事均一生物微球和微囊的制备及其在生化工程和医学工程中的应用,研究和开发用于药物载体、免疫佐剂(疫苗递送系统)、细胞培养微载体等创新产品。

魏炜研究员 2011年获中国科学院过程工程研究所博士学位,获国家“优秀青年科学基金”(2016)等人才项目,目前任中国科学院过程工程研究所生化工程国家重点实验室主任助理。研究领域主要聚焦于仿生剂型工程,重点基于蛋白、细菌、细胞等天然对象,对载体进行仿生设计,并发展新的制备过程,借助仿生对象体内固有途径实现药物精准递送,应用于抗肿瘤、疫苗、组织修复等领域。

吕岩霖副研究员 2018年获中国科学院大学博士学位,主持和参与国家基金委、中科院项目3项,目前任中国科学院过程工程研究所生化工程国家重点实验室学术秘书。主要聚焦于光活性纳米材料的仿生设计与肿瘤诊疗方面的研究。
供稿:原文作者
编辑:《颗粒学报》编辑部
