
A new track for antibacterial treatment: Progress and challenges of using cytomembrane-based vesicles to combat bacteria (Open Access)
谢佳璇,刘旋*,刘刚*
Keywords: Cytomembrane-based vesicles; Bacterial resistance; Antibacterial therapy; Drug delivery
DOI: 10.1016/j.partic.2022.10.006
耐药细菌,尤其是超级细菌的反复出现,导致了越来越难以治疗的复杂细菌感染,当今世界迫切需要新的抗菌替代疗法来降低抗生素耐药引起的发病率和死亡率。进入21世纪以来,生物疗法的迅猛发展为解决这一具有挑战性的任务打开了新的思路。作为一种新型生物材料,基于细胞膜的囊泡(MVs)因其固有的生物相容性、设计灵活性以及与生物分子或周围环境的相互作用能力而在抗菌治疗中受到广泛关注。基于此,近日,厦门大学分子影像暨转化医学研究中心刘刚教授研究团队受邀在PARTICUOLOGY发表题为“A new track for antibacterial treatment: Progress and challenges of using cytomembrane-based vesicles to combat bacteria”的综述文章,总结了近年来MVs在抗菌领域的研究进展,并对MVs在临床转化中可能面临的困难进行了分析梳理。
本文已OA,欢迎感兴趣的读者扫描下方二维码进入ScienceDirect官网阅读、下载!

1. 研究背景
作为悬在人类健康头顶上的达摩克利斯之剑之一,细菌感染无时无刻威胁着生命的正常运行。一直以来,抗生素都是抵抗细菌感染的前线兵团,然而它的滥用造成了当今世界细菌耐药性的疯狂进化,使得悬剑之绳又细了几分。近年来,为了突破耐药困境,研究者们开始将目光投注到方兴未艾的纳米医学领域。基于细胞膜的囊泡(Cytomembrane-based Vesicles, MVs)因其固有的生物相容性、设计灵活性以及与生物分子或周围环境的相互作用能力而在抗菌治疗中颇受研究者青睐。本文综述了MVs的特性和生理功能,重点介绍了其抗细菌感染的潜力,包括毒素清除、免疫调节、抗生素递送和物理治疗,并探讨了MVs在未来抗菌治疗临床应用的可能性及挑战。
2. 基于细胞膜的囊泡(MVs)的简介
MVs是指由脂质膜包裹形成的纳米或微米级囊泡,其膜来源于真核或原核细胞。作为脂质体的天然类似物,MVs可作为通用运输系统,运输蛋白质、脂质和遗传物质等各类分子货物。主要的MVs种类有细胞外囊泡(包括外泌体、微泡、凋亡小体)、细菌外膜囊泡(Outer Membrane Vesicles,OMVs),以及人工工程化囊泡。相较于来源于天然细胞膜的前两者,工程化囊泡可根据实际应用需要,运用化学修饰、物理作用、受-配体结合、基因工程等手段,赋予其特异靶向、特殊药物递送等功能,为诊断、治疗等领域提供了有力平台。
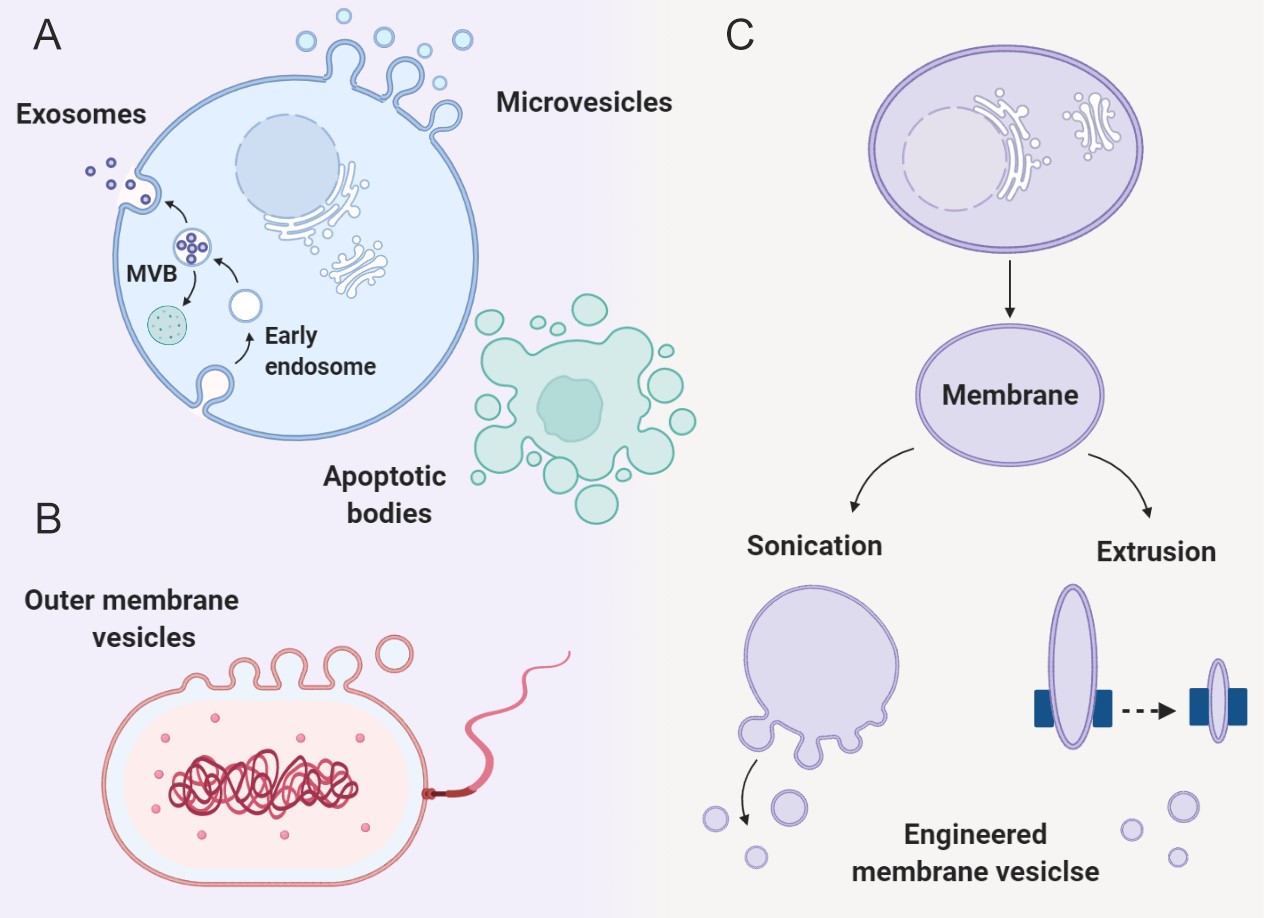
图1. 基于细胞膜的囊泡
3. MVs的抗菌应用
3.1 毒素清除
成孔毒素(PFTs)是由致病菌分泌的毒力因子,广泛存在于各种细菌感染,可增强病原体的毒性;其主要作用机理是通过在细胞膜上形成孔道结构,改变细胞通透性进而裂解细胞。基于PFTs与细胞膜的作用特性,利用MVs作为诱饵,经由被动吸引效应,可有效吸附PFTs。红细胞膜来源的MVs在多种细菌感染中,都表现出了显著的毒素清除效果。同时,在MVs中装载微环境响应释放的抗生素内核,还可进一步释放近距离杀伤细菌病原体。
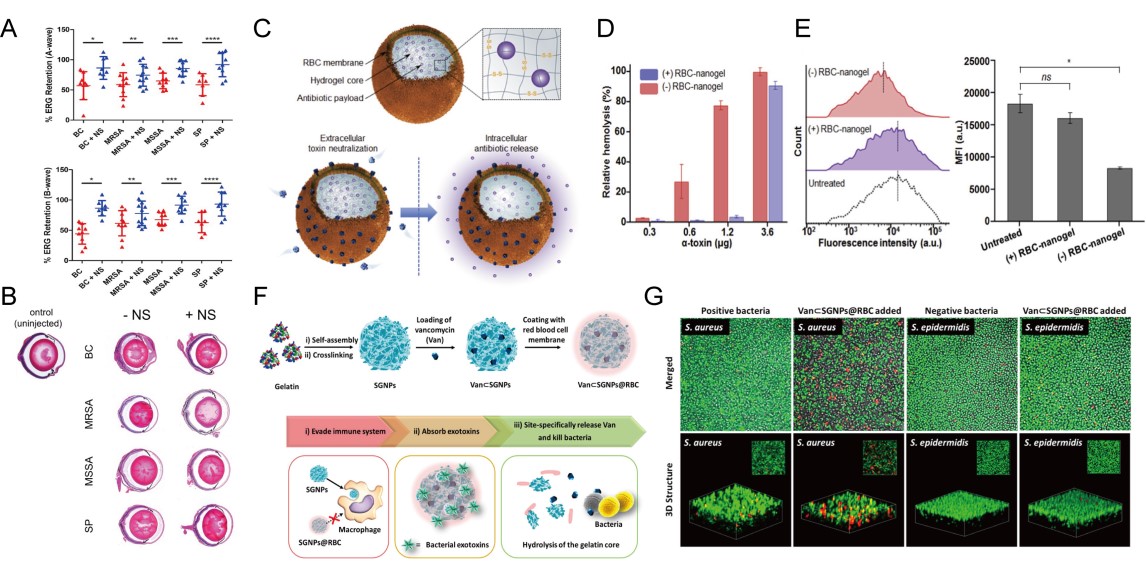
图2. MVs中和毒素
3.2 免疫调节
机体的免疫作用在抗菌治疗过程中一直起着重要作用,诸多研究都已报道MVs可参与免疫调节反应。实际上,来源于细胞的MVs包含了丰富的免疫信息,比如免疫细胞或者肿瘤细胞所衍生的MVs自动继承了二者的免疫特性,在免疫调节中直接起到积极或消极作用。以此为基础,衍生于中性粒细胞的MVs携带Resolvin D1和抗生素Ceftazidime,既可抑制病原体引起的炎症反应,又可以杀伤细菌,一举两得。而OMVs因其自带天然抗原,作为疫苗可以有效激活机体的免疫反应,预防细菌感染,比如广泛运用于预防脑膜炎奈瑟菌的疫苗4CMenB即包含新西兰MenB 菌株(B:4:P1.7–2.4)的OMVs。此外,通过基因工程在细菌膜表面过表达免疫抗原,获得的OMVs也可有效触发高水平的特异性抗体产生。
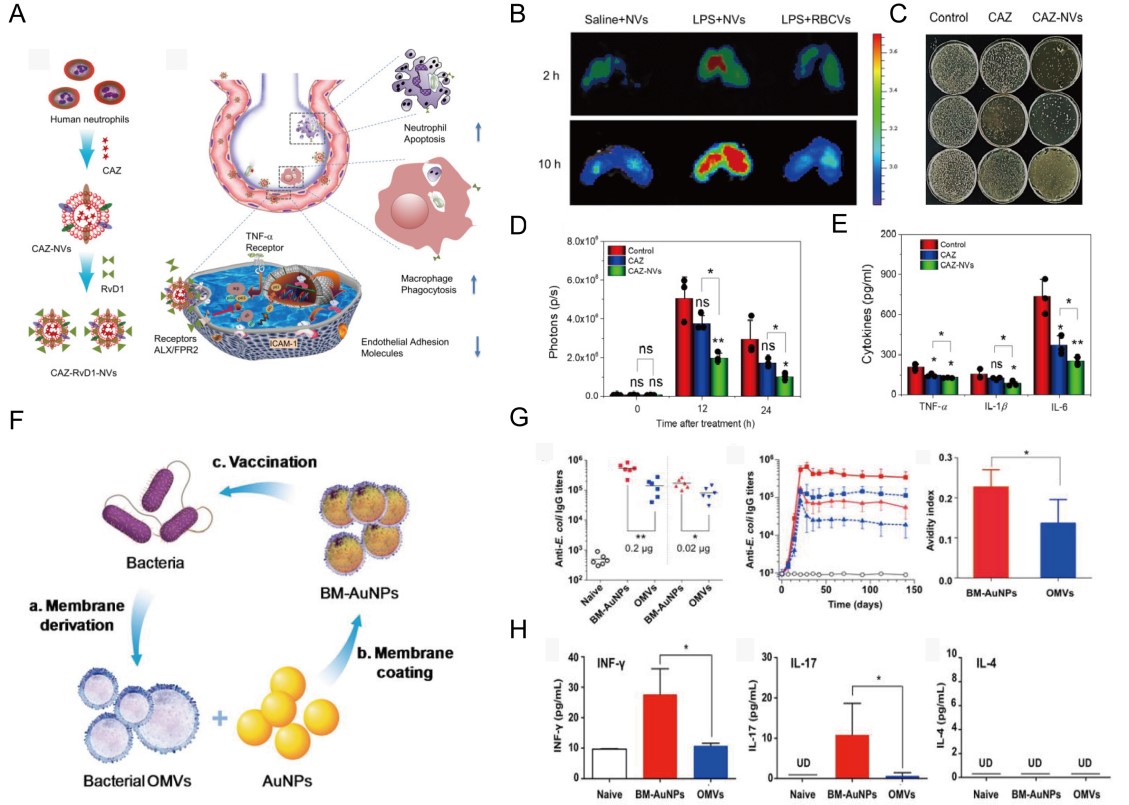
图3. MVs调节免疫系统清除细菌
3.3 抗生素递送
细菌耐药的抵抗机制之一就是使用各种手段将药物隔离在菌体之外,或者将进入菌内的药物重新泵出,因此,在细菌耐药的情况下,绝大多数药物无法进入细菌。研究证明使用MVs将抗菌药物输送到细菌细胞中,可有效增加药物吸收并降低耐药性,克服治疗障碍。自然界中,不同种属的细菌之间存在着竞争关系,OMVs则是双方生存作战的武器,这就为细菌治疗提供了一个思路,使用针对目的菌株的敌对OMVs来杀伤耐药菌,获得鹬蚌相争渔翁得利的效果。此外,有研究报道,某些细菌接受抗生素刺激后会产生OMVs包裹抗生素并分泌到胞外,利用这一特性可以建立细菌平台,生产大量包含抗生素的OMVs,然后反其道而行之,将其施与其他耐药菌,抗菌效果显著。
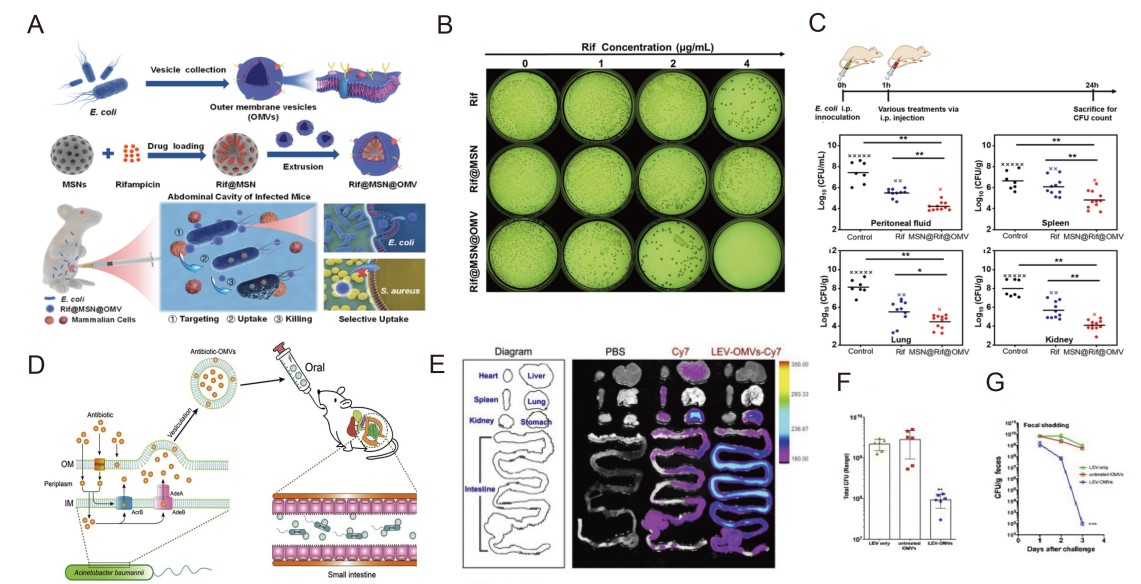
图4. MVs递送抗生素杀伤细菌
3.4 物理治疗
物理抗菌疗法是一种基于机械、电、声和其他手段治疗细菌抗生素耐药性的策略。这种物理杀灭方法通过机械拉伸或干扰微生物代谢来破坏细菌的结构和功能,大大减少了微生物耐药性的出现,在治疗耐药感染方面显示出了一定前景。声动力疗法(SDT)利用超声波激发声敏剂,触发电子转移,使水和氧发生反应并产生抗菌活性氧(ROS)。然而声敏剂的亲水性和稳定性差,大大削弱了它们的抗菌性能。为了保护声敏剂的结构功能,使用膜表面展示毒素抗体的MVs装载声敏剂邻四(4-磺胺苯基)卟啉,借助抗原抗体特异性结合,可以将MVs精准靶向细菌部位,在超声激活条件下,产生ROS协助抗菌,由于这种声敏剂具有发光属性,故兼具治疗可视化功能。
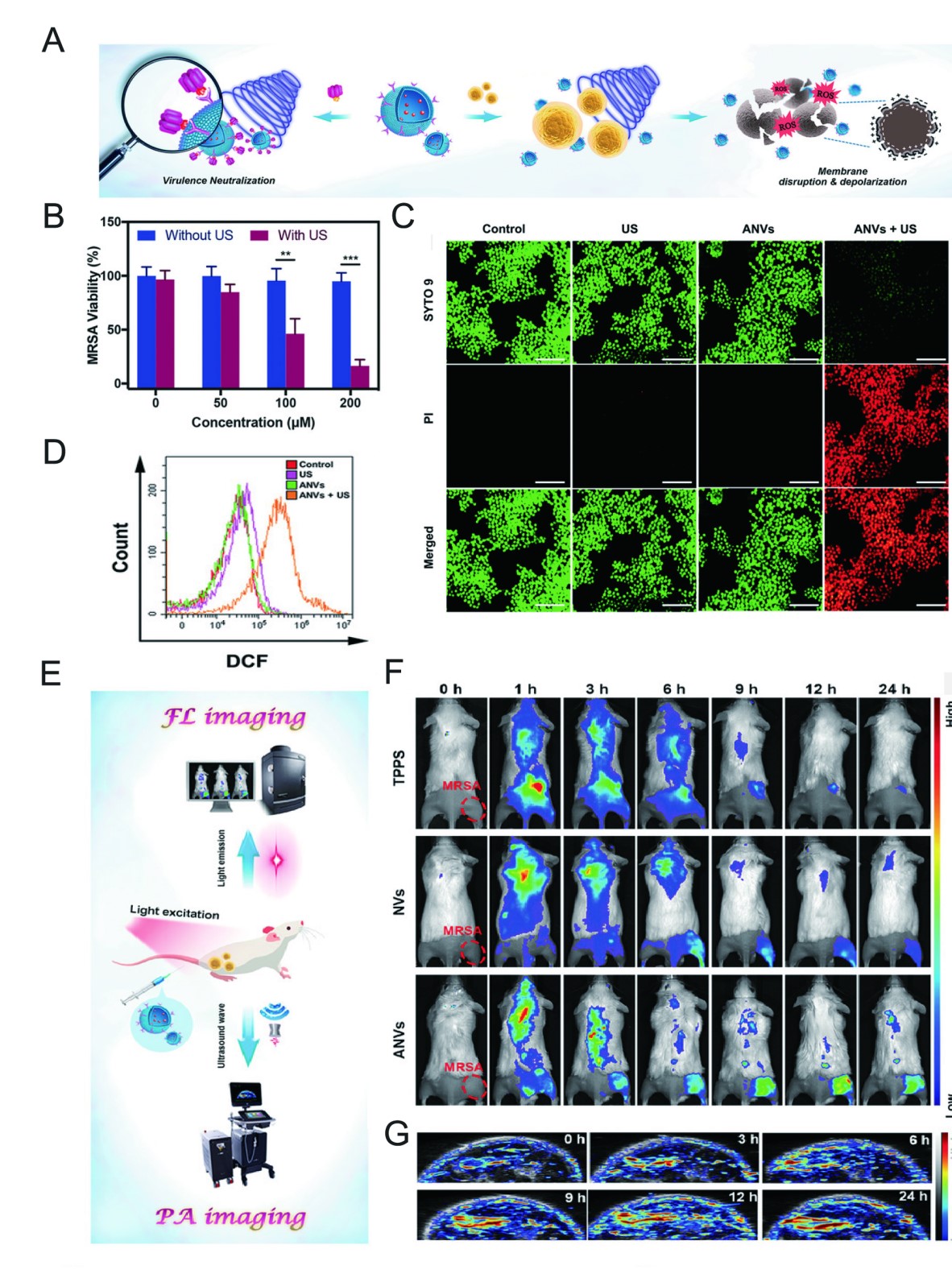
图5. MVs用于物理抗菌疗法
4. 总结
持续的细菌感染导致了全球高发病率和死亡率。近年来,纳米医学在抗菌治疗方面取得了很多进展,为解决细菌耐药性创造了新的方案。MVs进可载药中和毒素,退可调动免疫联合物理疗法,具有很强的可塑性和潜力。然而,作为细胞衍生的复杂有机结构体,注定了临床转化路上会面临诸多挑战:(1)复杂的生物大分子成分自带免疫原信息,可能引起免疫排斥;(2)MVs结构的均一性和量产无法精确控制,制备工艺仍需进一步优化;(3)MVs的功能稳定性有待评估,比如基因重组后目的蛋白的表达效率难以质控等。虽然如此,但是相信随着物理、化学和基因工程技术领域的蓬勃发展,MVs成为一个广谱抗菌的交叉应用平台终有实现的可能。
5. 通讯作者

刘刚教授,博导,厦门大学南强特聘教授,国家杰出青年基金及国家优秀青年基金获得者,中组部万人计划青年拔尖人才,中国生物医学工程学会理事及青委会副主任委员,中国生物材料学会理事,中华医学会放射学分会分子影像学组副组长,中国医师协会介入医师分会介入医学工程与生物技术学组副组长,中国生物物理学会材料生物学与智能诊疗技术分会副会长。长期致力于分子影像学及药物递送系统研究,指导研究生在Nat. Nanotechnol.、Nat. Commun.、Sci. Adv.、PNAS、JACS、Adv. Mater.等国际知名杂志发表论文200余篇(H因子71,引用超过1.5万次),参编国家规划教材5部,英文专著16部。获得国家专利授权20余项,其中6项进行了企业技术转移及临床转化并获国家或省级科技奖7项。
相关代表性工作:
(1) Metal-based nanoparticles for cardiovascular disease diagnosis and therapy, 2023, Particuology, 72: 94-111, DOI: 10.1016/j.partic.2022.03.002
(2) Cell membrane-encapsulated nanoparticles for vaccines and immunotherapy, 2022, Particuology, 64: 35-42, DOI: 10.1016/j.partic.2021.04.017
(3) Repurposing ICG enables MR/PA imaging signal amplification and iron depletion for iron-overload disorders, 2021, Science Advances 7(51):eabl5862, DOI: 10.1126/sciadv.abl5862
(4) An exploratory human study of superstable homogeneous lipiodol–indocyanine green formulation for precise surgical navigation in liver cancer, 2022, Bioengineering & Translational Medicine, DOI: 10.1002/btm2.10404
(5) A nanovaccine for antigen self-presentation and immunosuppression reversal as a personalized cancer immunotherapy strategy, 2022, Nature Nanotechnology 17(5): 531–540, DOI: 10.1038/s41565-022-01098-0
供稿:原文作者
编辑:《颗粒学报》编辑部
文章信息
Xie, J., Liu, X., & Liu, G. (2023). A new track for antibacterial treatment: Progress and challenges of using cytomembrane-based vesicles to combat bacteria. Particuology, 78, 136-146. https://doi.org/10.1016/j.partic.2022.10.006
