
Modulation of reactive oxygen species to enhance sonodynamic therapy (Open Access)
刘笑妤,潘雪婷,王朝辉,刘惠玉*
Keywords: Reactive oxygen species; Sonodynamic therapy; Sonosensitizers; Oxidative stress; Combination therapy
DOI: 10.1016/j.partic.2022.08.001
在光动力治疗、化学动力治疗、声动力治疗等多种依赖活性氧作用的疾病治疗方式中,超声介导的声动力治疗因为其无创性、良好的生物耐受性和高组织穿透深度脱颖而出,受到研究者们的关注。在过去的30多年,声动力治疗被广泛应用于多种疾病治疗中,如心血管疾病、癌症和细菌感染。
活性氧作为细胞代谢过程的一类重要产物和声动力治疗过程的重要作用因素,主要种类包括超氧阴离子、羟基自由基、单线态氧、过氧化氢等。活性氧具有双重调控作用。当细胞中活性氧的产生超过了细胞抗氧化防御系统的能力时,大量的活性氧积累会破坏细胞损伤修复机制,引起细胞内DNA突变,对蛋白质和脂质造成不可逆的损伤,促进疾病的发展。然而,毒性水平的活性氧也会诱导细胞死亡从而抑制疾病的发展。因此,调节局部细胞活性氧水平对疾病治疗具有重要意义。
基于此,北京化工大学刘惠玉教授团队在PARTICUOLOGY上发表综述文章,系统总结了用于增强声动力治疗效果的活性氧调节策略。该文章首先介绍了声动力治疗过程中活性氧的产生机制。随后总结和讨论了通过合理设计声敏剂和调节疾病微环境以增强活性氧产生的策略。最后,提出了声动力治疗与其他基于活性氧的治疗方式联合应用的潜力。
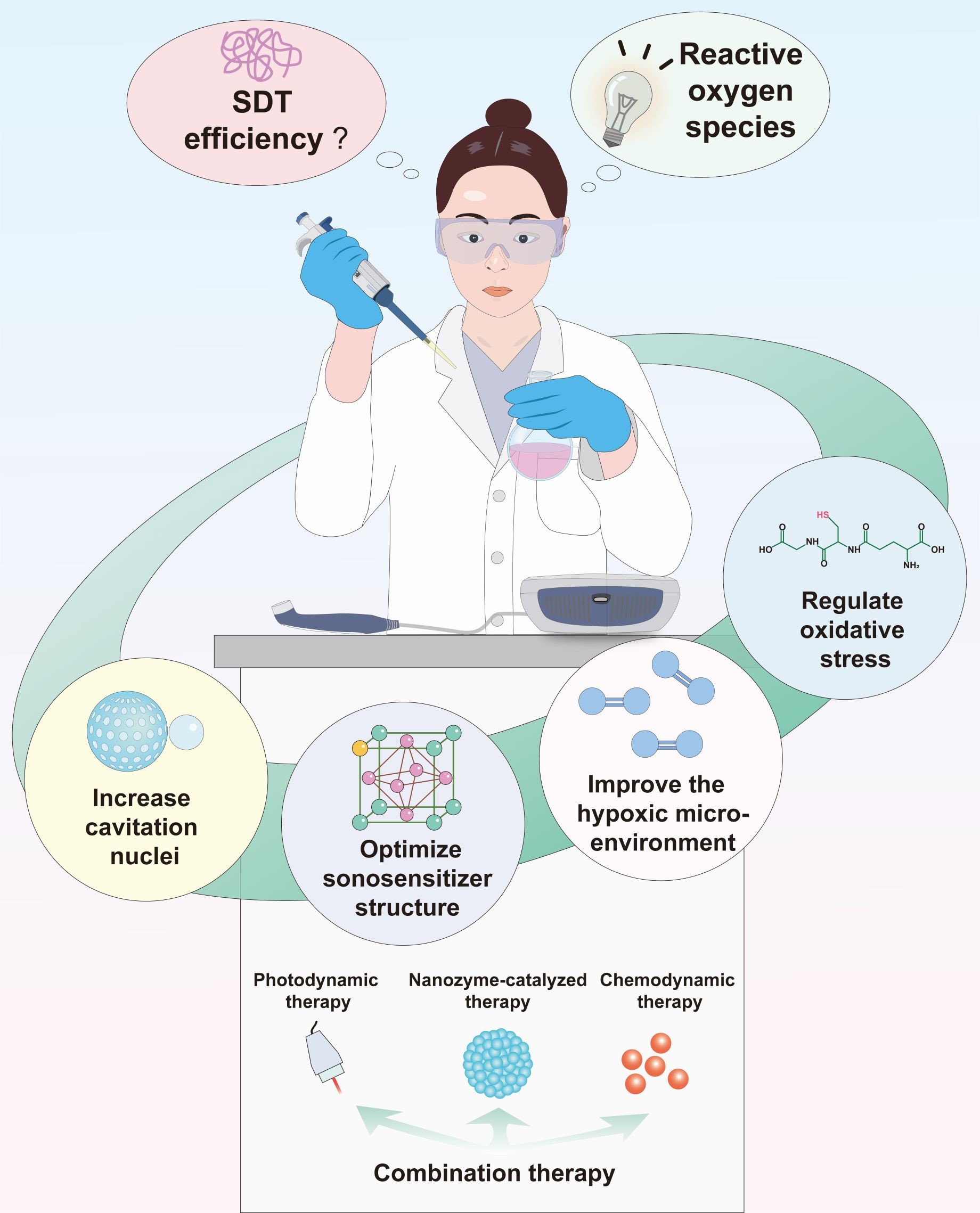
图1. 声动力治疗中活性氧生成的调控策略。
本文已OA,欢迎感兴趣的读者扫描下方二维码进入ScienceDirect官网阅读、下载!

1 声动力治疗中活性氧的产生机制
作为声动力治疗中的重要因素,活性氧的产生机制受到了广泛关注。本节重点介绍了声动力治疗过程中的活性氧产生机制。一般认为,声动力治疗中活性氧的主要产生机制是空化效应和声致发光。此外,还简要介绍了超声辐照下压电材料产生活性氧的机理——压电效应。
1.1 空化效应
空化效应的机理较为复杂。非惯性空化和惯性空化是空化效应的两种类型,其中惯性空化会产生活性氧。惯性空化的过程分为三个阶段:成核、气泡生长和内爆,过程中伴随着发光、高温、高压、放电和微射流等现象。该过程可以被具体解释为:当超声强度超过一定压力阈值时,气泡膨胀超过预定的共振尺寸,使得其失去稳定性后流体向内撞击,引起气泡破裂和内爆,能量以热能的形式释放,进而引发声化学反应产生活性氧和声致发光现象。
1.2 声致发光
声致发光是空化气泡由于超声的作用而突然坍塌时发生的发光现象。声致发光产生活性氧的机制仍在不断探究中,目前有以下解释:
(1)空化气泡的内爆产生高能光子,声致发光下的声敏剂分子或某些内源性化合物被该能量从基态激活到激发态。处于激发态的声敏剂可以将其激发能量转移到周围的基态氧分子中,从而产生单线态氧。
(2)对于半导体声敏剂,释放的能量使价带中的电子跃迁到导带,同时在价带中留下相应的空穴。电子和空穴在电场中迁移到粒子表面并在其中形成电子-空穴对,随后介导氧气和水的氧化还原反应,从而产生超氧阴离子、单线态氧和羟基自由基。
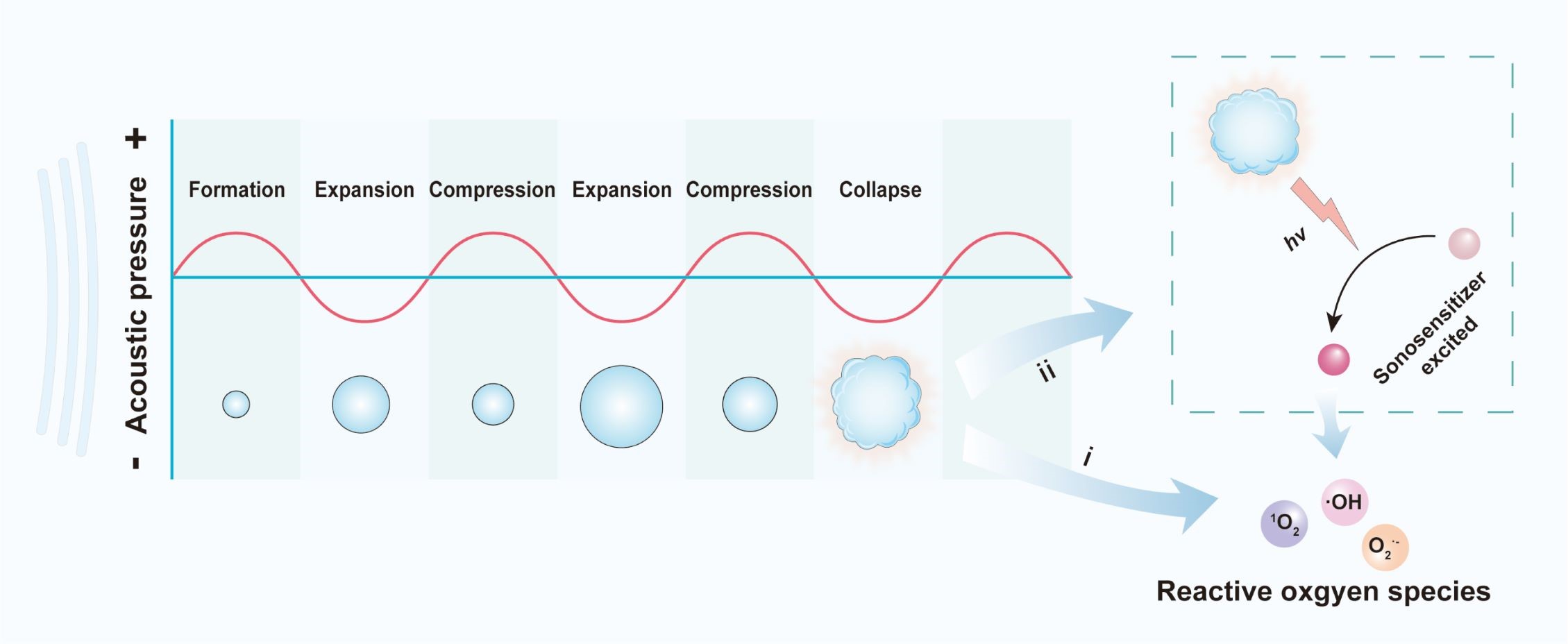
图2. 超声辐照下活性氧产生的常见机制。
1.3 压电效应
压电材料基于其自身固有的压电效应,可以在超声辐照下产生活性氧。超声辐照下压电材料产生活性氧的机理可分为机械应力介导的压电催化和声致发光介导的光催化。
压电催化是由机械应力引起的电荷重新定位引发的。在一定的超声强度下,处于电荷平衡状态的极化压电材料由于压电效应的压应力(负应变)释放屏蔽电荷形成自由电荷,并与水结合生成活性物质。在周期性的超声机械应力和电解质环境下,压电材料通过屏蔽电荷的释放和吸附来保持电荷平衡,进而提供持续的电荷,产生超氧阴离子和羟基自由基。而在声致发光介导的光催化中,声致发光释放的能量激发压电材料中的电子从价带跃迁到导带,并且电子-空穴对被分离并产生内部电场。分离的电子和空穴迁移到压电材料表面,产生压电势来驱动氧化还原反应,与周围的分子发生氧化还原反应生成活性氧。基于压电效应,为新型声敏剂的设计和声动力治疗新机制的探索提供了新的方向。
2 声动力治疗中的活性氧调节
细胞依靠其抗氧化防御系统来维持氧化还原稳态和正常的生理活动。因此,调整其内部活性氧水平、破坏氧化还原稳态或破坏抗氧化防御机制以诱导细胞功能障碍是重要的疾病控制策略。疾病区域的活性氧水平可能决定最终的治疗效果。基于此,本节介绍了基于声敏剂设计和疾病微环境调节的活性氧调节策略增强活性氧产生。
2.1 声敏剂设计
2.1.1 增加空化核
空化核对空化有显著的促进作用。内源性空化核的缺失导致空化阈值升高,需要高强度超声才能获得有效的声动力效果。通过在声敏剂中引入外源性空化核,结合低强度超声,可以有效提高空化效应和疾病治疗效率。改变声敏剂的表面性质以提供空化成核位点是增强空化效应的有效途径。此外,随着声敏剂的深入探索,加载气体源增加空化核的合成策略也得到了广泛应用。
2.1.2 声敏剂结构优化
在二氧化钛等传统声敏剂中,电子和空穴的快速复合导致ROS产生效率低下和存活时间短,限制了其在疾病治疗中的作用。通过优化声敏剂的结构,减少电子-空穴复合,提高载流子迁移效率,可以显著增加活性氧的产生。目前使用的方法包括元素掺杂、缺陷构建、异质结等。
2.1.3 压电材料作为声敏剂
压电材料在外力作用下产生相反电荷的特殊性使其具有多种应用方向。表面电荷的产生有利于声动力治疗中活性氧的产生。因此,压电材料作为声敏剂的适用性也得到了广泛的研究。
2.2 疾病微环境调节
2.2.1 改善乏氧微环境
肿瘤微环境的缺氧状态严重阻碍了声动力治疗的效率。改善乏氧微环境已成为提高声动力治疗效果的主要研究方向,包括氧气运输和原位氧气产生等多种方法。
2.2.2 氧化应激调节
肿瘤组织为抵抗高水平活性氧带来的损害,通常会上调抗氧化防御系统。这也是声动力治疗过程中肿瘤部位活性氧水平未达到预期的重要原因。因此,氧化应激调节是癌症治疗的重要策略。谷胱甘肽是细胞中最丰富的内源性抗氧化剂,可维持生物系统内的氧化还原平衡。过量的谷胱甘肽可以清除细胞毒性活性氧,增强癌细胞对活性氧的抵抗力。因此,消耗谷胱甘肽和抑制谷胱甘肽合成是增强活性氧含量的有效策略。
3 联合治疗
3.1 与光动力治疗结合
由于组织穿透力有限,光动力治疗难以应用于深部疾病的治疗。超声因其独特的深层组织穿透能力可以很好地弥补这一缺陷,因此声光动力疗法作为一种新的治疗方法已被广泛研究。声动力治疗和光动力治疗联合使用进一步增强了活性氧的产生,可以在降低致敏剂剂量的同时提高细胞毒性,达到更好的治疗效果。
3.2 与纳米酶催化治疗结合
纳米酶是一类具有酶催化特性的纳米材料。纳米酶具有与肿瘤微环境相互作用的潜力,同时具有更高的稳定性,可用作肿瘤治疗中的治疗剂。纳米酶具有多种催化活性,例如具有类过氧化氢酶活性的纳米酶可产生氧气,而具有类过氧化物酶活性的纳米酶可产生羟基自由基。因此,声动力治疗与纳米酶结合能够产生更多的活性氧,实现高效的疾病治疗。
3.3 与化学动力学治疗结合
化学动力学治疗可以使用具有芬顿或类芬顿活性的纳米材料催化过氧化氢生成羟基自由基,从而引发肿瘤细胞的死亡。可应用于声动力治疗和化学动力学治疗的纳米药物在联合作用下增强了活性氧的产生,从而实现更深的组织渗透。因此,将声动力治疗和化学动力学治疗相结合是一种很有前途的疾病治疗方法。
4 总结与展望
近年来,声动力治疗作为一种有效的疾病治疗方式被广泛研究。目前,声敏剂的研发如火如荼,但大多数仅在实验室实验中表现出优异的治疗效果,在临床应用中面临重大限制。纳米粒子所具有的复杂的制备工艺、对健康组织的毒性和体内代谢困难是亟待解决的问题。目前还存在以下问题:(1)声动力治疗的生物学机制尚不清楚;(2)活性氧的快速转化使得活性氧在体内的生物学效应不确定;(3)声动力治疗中各参数的标准差异过大;(4)声敏剂的药物靶向性和环境响应性较差;(5)单一治疗方式的疾病治疗效果有限。通过回顾该领域的最新进展,我们相信对声动力治疗增强策略的理解和探索将有助于声动力治疗的进一步发展和临床转化。
5 通讯作者简介

刘惠玉,北京化工大学教授,博士生导师,国家优秀青年基金和牛顿高级学者基金获得者,国家自然科学奖函评专家,科技部“重点专项”会评专家。2007年7月博士毕业于中国科学院理化技术研究所并留所工作,2013年9月至2014年9月在美国加州大学洛杉矶分校作访问学者,2015年11月起任北京化工大学教授。研究领域为生物医用材料,在Angew. Chem. Int. Ed., Adv. Mater., ACS Nano等国际期刊发表论文97篇,总引用8400余次,ESI高被引论文11篇,H指数43,授权发明专利12项。担任Wiley旗下Exploration期刊副主编,Materials & Design编委,Mater. Express编委、《无机化学学报》青年编委。中国医药生物技术协会纳米生物技术分会常务委员。曾获北京市医学科技奖二等奖(排名2),中国科学院卢嘉锡青年人才奖,北京市科技新星等荣誉称号。于2019、2020年连续入选Elsevier&Stanford公布的“标准化引文指标全科作者数据库”全球10万全科科学家年度影响力名单。
供稿:原文作者
编辑:《颗粒学报》编辑部
